Impacto de la Infección por VIH en Lesiones Intraepiteliales de Cuello Uterino
Autores:
Villalba Natalia1, Farias Miño Guido1, Grimaldi Úrsula1, Cora Eliseth Martha1, Fleider Laura1
Resumen
El objetivo de esta investigación tiene como propósito determinar el impacto del virus de la inmunodeficiencia humana (VIH) en lesiones precursoras del cáncer de cuello de útero en pacientes atendidas en el Hospital escuela de agudos Dr. Ramón Madariaga de la ciudad de Posadas de la provincia de Misiones, centro de referencia y derivaciones en el periodo desde el primero de enero de 2017 al treinta uno de diciembre de 2021.
El material y métodos se basaron en un estudio de tipo Descriptivo y Retrospectivo. Los documentos en los que se basó la recolección de datos se obtuvieron de las historias clínicas de las pacientes a las cuales fueron realizadas dicha práctica que se atendieron en el hospital, en el período establecido desde enero del 2017 a diciembre del 2021. El universo estudiado es de un total de 25 pacientes.
Las lesiones precursoras del cáncer de cuello uterino están asociadas a la infección persistente por el virus del papiloma humano (HPV) siendo los más prevalentes 16 y 18. En mujeres VIH + tienen una mayor persistencia de los genotipos de alto riesgo, progresión acelerada y menor regresión espontánea por la alteración del sistema inmunológico. Se abordará sobre el impacto en la coinfección analizando la fisiopatológica, la epidemiología en América Latina y las medidas actuales de tamizaje, tratamiento y prevención destacando la necesidad de un manejo multidisciplinario para poder realizar un diagnóstico, tratamiento y seguimiento oportuno.
Con respecto a nuestro centro de investigación se pudo concluir que aquellas pacientes VIH + con buen estado inmunológico, cumplimiento adecuado del tratamiento antirretroviral y quirúrgico, y el no abandono del seguimiento tiene el mismo impacto que aquella paciente sin infección por VIH en el desarrollo de lesiones precursoras de cuello uterino.
Planteamiento del Problema
Debido a un aumento mundial en la infección por VIH y ser considerado como un problema de salud prioritario, se decidió evaluar el impacto de la infección por VIH en el desarrollo de lesiones precursoras de cáncer de cuello uterino con el fin de hacerle frente a esta entidad.
Formulación del Problema
¿Cuál es el impacto del VIH en lesiones precursoras de cáncer de cuello uterino en el hospital escuela de agudos Dr. Ramón Madariaga desde el periodo enero de 2017 hasta diciembre del 2021?
Justificación
El cáncer de cuello uterino es una manifestación clínica del SIDA, ya que las mujeres que viven con el VIH y contraen el virus del papiloma humano tienen más probabilidades de desarrollar lesiones pre invasivas; que, si no se tratan, pueden convertirse rápidamente en cáncer invasivo. Las mujeres que viven con el VIH tienen seis veces más probabilidades de desarrollar cáncer de cuello uterino invasivo. Se ha apreciado que la infección por el virus del papiloma humano incrementa significativamente el riesgo de transmisión del VIH tanto en los hombres como en las mujeres.
La investigación tiene como fin identificar la repercusión que tiene el VIH en lesiones precursoras en mujeres atendidas en el Hospital escuela de Agudos Dr. Ramón Madariaga de la localidad de Posadas de la provincia de Misiones, con el fin de poder diagnosticar precozmente e intervenir de forma oportuna.
Objetivo General
- Impacto del VIH en lesiones precursoras de cáncer de cérvix en el Hospital escuela de agudos Dr. Ramón Madariaga de la localidad de Posadas, provincia de Misiones, desde el periodo primero de enero de 2017 hasta treinta y uno de diciembre del 2021.
Objetivos Específicos
- Establecer la edad promedio de lesiones precursoras en pacientes HIV positivas.
- Conocer el tipo de lesión más frecuente según las clasificaciones del proyecto LAST.
- Definir la repercusión del estado inmunológico de la paciente HIV+ y el desarrollo de la lesión precursora.
- Determinar la realización de conización cervical o no.
- Verificar el uso correcto del tratamiento antirretroviral .
- Evaluar la asociación del tiempo de evolución de la lesión precursora y el tratamiento antirretroviral.
- Determinar la eficacia del seguimiento en conjunto de su condición ginecóloga e inmunológica.
- Evaluar nuevas lesiones precursoras posterior al tratamiento ginecológico.
Marco Teórico
El virus de la inmunodeficiencia humana (VIH) se descubrió en 1983 por Françoise Barré-Sinoussi y Luc Montagnier en el Instituto Pasteur de París y posteriormente en 1984 por el propio grupo de Robert Gallo en el Instituto Nacional de cáncer en Bethesda, EE. UU y en 1986 se acordó la denominación de VIH.
El VIH pertenece a los lentivirus y se divide en dos tipos: VIH-1 y VIH-2 que tienen un 40-50% de homología genética y una organización genómica similar. El VIH-1 causo la pandemia mundial de sida, el VIH-2, aunque también puede producir sida, se considera menos patogénico y transmisible. (Delgado, 2011)
Estructura del VIH
El VIH-1 es esférico con un diámetro de 100-120nm presenta una envoltura con una bicapa lipídica tomada de la membrana de la célula humana durante el proceso de gemación de nuevas partículas. En esta envoltura se encuentran presentes algunas proteínas de la célula huésped y muy significativamente Env, la glicoproteína de envoltura del VIH. Esta se ancla en la membrana y se encuentra formada por tres moléculas llamadas glicoproteína 120 (gp120), en la zona más externa, y un tronco de una estructura transmembrana que consta a su vez de tres moléculas llamadas glicoproteína 41 (gp41). La estructura y funcionalidad de Env son claves para entender aspectos importantes de la biología del VIH-1, tales como la interacción con receptores celulares (tropismo) y la evasión inmune.
Los factores relacionados con la dificultad de neutralizar la infección por VIH-1 se relacionan con Env: 1) 5 regiones hipervariables en la zona más externa de gp120, 2) alto nivel de glicosilación de Env con más del 50% de su masa en azúcares (N-glicosilación), que impide la unión de anticuerpos y 3) enmascaramiento conformacional donde el sitio de unión con los co-receptores (CCR5 o CXCR4) no existe hasta que se organiza espacialmente después del cambio en la conformación de gp120 inducido por la interacción con CD4, debido a esto es su poca susceptibilidad a la neutralización mediada por anticuerpos.
El gen gag codifica las proteínas estructurales: la proteína de matriz p17, en el interior de la membrana y la proteína de la cápside p24, que, por polimerización, forma una estructura nuclear cónica que contiene un complejo proteína-ácido nucleico formado por dos copias del ARN genómico del VIH-1, la nucleoproteína p7 y la transcriptasa inversa p66 (RT). El gen Pol codifica las tres enzimas necesarias para el ciclo infectivo del virus: la proteasa (PR), la transcriptasa inversa (RT) y la integrasa (IN) (fig. 5). Además, el VIH-1 tiene otros seis genes accesorios: tat, rev, nef, vif, vpu y vpr con un papel muy importante en el ciclo biológico del virus.
Tat y Rev son proteínas reguladoras intranucleares y se unen a regiones específicas del ARN viral. La proteína Tat es un potente activador de la transcripción y es esencial para la replicación del virus. Rev es un factor de exportación nuclear que facilita la salida al citoplasma de los ARN mensajeros largos antes de ser procesados en el núcleo y permite así la traducción y expresión de las proteínas estructurales. Nef inhibe regulación de CD4 y moléculas HLA de clase I en la superficie de las células infectadas siendo mecanismo de escape importante al evadir un ataque mediado por linfocitos CD8+ citotóxicos. Nef interfiere con la activación del linfocito T al unirse a varias proteínas que intervienen en las vías de transducción de señales intracelulares. Vpr es importante para el transporte al núcleo del complejo viral pre-integración, inmediatamente después de la entrada del virus a la célula lo que permite al VIH-1, a diferencia de la mayoría de los retrovirus, infectar células que no estén dividiéndose.
El VIH-1 se transmite principalmente por contacto sexual a través de la gran concentración de partículas en semen y fluidos genitales. Pero también puede hacerlo por medio de transfusiones, trasplantes y de manera vertical entre otras. (Delgado, 2011)
Reservorio Viral del VIH
El linfocito T CD4+ infectado es destruido en un plazo de 24 horas después de que el virus complete su ciclo infeccioso; sin embargo, algunas células infectadas no son destruidas y pueden volver a un estado quiescente tras la infección, albergando el virus latente con una vida media de aproximadamente 4 años (linfocitos T CD4+ de memoria en reposo). Por lo que al suspender el tratamiento antirretroviral la replicación se reanuda a expensas de este reservorio. (Delgado, 2011) (CDC, 2025)
El VIH es un virus que ataca el sistema inmunitario del cuerpo. No existe una cura eficaz actualmente ni vacunas para ellos por lo que la falta de tratamiento con los medicamentos para el VIH puede acelerar la progresión de la enfermedad a SIDA (síndrome de inmunodeficiencia adquirida). Las personas con infección por el VIH con tratamiento eficaz pueden tener una vida larga y saludable. (CDC, 2025)
Fases de Progresión del VIH
Con los avances en el tratamiento, la progresión a la fase 3 es menos común hoy en día de lo que era al principio. Existen 3 fases:
- Fase 1: Infección aguda por el VIH
Gran viremia siendo muy contagiosas. Algunas personas tienen síntomas similares a los de la influenza. Esta es la respuesta natural del cuerpo a la infección. Se diagnostica con las pruebas de antígenos y anticuerpos, o con las pruebas de ácido nucleico.
- Fase 2: Infección crónica por el VIH
Fase de infección asintomática o de latencia clínica. El virus se encuentra activo, pero con reproducción baja. Son asintomáticos y puede durar décadas. En esta fase se produce aumento de carga viral y se disminución de recuento de células CD4.
- Fase 3: Síndrome de inmunodeficiencia adquirida (SIDA)
Depleción del sistema inmune con la facilidad de contraer enfermedades oportunistas, los recuentos de células CD4 caen por debajo de 200 células/mm3 Sin tratamiento, estos sobreviven aproximadamente tres años, por lo general.
Un estudio sobre esperanza de vida ha revelado que las personas con el HIV que inician pronto su tratamiento antirretroviral y disponen de acceso a una buena atención sanitaria pueden esperar tener una esperanza de vida similar a sus iguales sin el VIH.
En el 2022 se diagnosticaron alrededor de 39 millones de personas con VIH a nivel mundial. En general, la prevalencia y la incidencia de las infecciones por HPV cervical, anal y oral son mucho más altas en estos pacientes y se asocian a HPV de alto riesgo (HPV- AR) y/o coinfección de diferentes genotipos de HPV.
Las infecciones cervicales fueron seis veces más altas en VIH+, mientras que en la región anal y oral fue el doble.
Una revisión sistemática desde 1986 al 2017 informó que el HPV anal aumentó 1.3-1.4 veces más en VIH+. Otro estudio determinó un aumento de 1.5 veces más frecuente, en hombres que tienen sexo con hombres (HSH).
El comportamiento sexual tiene mayor influencia en la prevalencia del estado del HPV que el VIH en sí. El sexo anal receptivo es un factor de riesgo bien documentado para la infección de HPV. (Bekana K. Tadese, 2025)
La carga de enfermedad anal es más prevalente en hombres que mujeres VIH+ con un riesgo de 2 a 7 veces más de lesión precursora anal y 2 a 25 en cáncer anal.
En cuanto a la distribución geográfica, influida por la disponibilidad de vacunas, baja aceptación, falta de cribados cervical y acceso reducido al sistema de salud, se observa un ascenso más marcado en África comparado con América del Norte y Europa. Dentro de los genotipos más frecuentes, el HPV 16 es más frecuente a nivel mundial.
Se observó que los genotipos incluidos en las vacunas 16-18-45 y la infección de múltiples genotipos 56-59 entre otros son más frecuente en la mujer con VIH+ .
Las tasas de incidencia de cáncer cervical son más altas en HIV jóvenes, siendo más prevalente en el rango etario entre 35 a 54 años para lesiones precursoras y de 30 a 45 años para patología maligna del cuello uterino sugiriendo una progresión más rápida. La edad varia notablemente, algunos autores establecen como edad media entre 25 a 39 años, otros en mayores de 36 años pico máximo a los 50 años, haciendo referencia a tasas más altas de persistencia de HPV debido a una disminución en la eliminación y reactivación de infección latente debido a inmunosenescencia.
Un recuento disminuido de CD4+ carga viral (CV) detectable y menor duración del tratamiento antirretroviral (TAR) son factores de riesgo para la coinfección con HPV y progresión de lesiones más rápidas.
En cambio, mujeres VIH+ con buen recuento de CD4+, CV no detectable y adecuado cumplimiento del tratamiento tiene el mismo riesgo que una paciente sin infección por VIH+.
En el estudio PICOPIV en Rumania, se estima que 3 de cada 4 mujeres con VIH tiene HPV. La prevalencia se relaciona con la carga viral y el número de recuento de CD4+. El incumplimiento del TAR asociado a CV detectable y CD4+ disminuidos aumenta las infecciones oportunistas y ciertos cánceres.
La prevalencia mundial de la infección por el virus del papiloma humano sin anomalía cervical es del 11-12% con tasas mayores en África, Europa y América Latina.
El centro europeo de monitoreo epidemiológico detectó lesiones anormales en el frotis cervical en 24,2%. El 68.42% de los VIH+ tenían HPV sin lesión cervical, el 26% presentaba lesiones precursoras. En Rumania los genotipos más frecuentes son el 31 y 56 difiriendo de los de a nivel mundial que son el HPV16 y HPV18. (Simona Claudia Cambrea, 2022)
Relaciones Sinergicas entre VIH y HPV
La infección por el virus del papiloma humano aumenta el riesgo del adquirir HIV. El riesgo por vía vaginal es 0.08% aumentado a 1.4% por vía anal. Claramente estas tasas pueden aumentar dependiendo de la CV, aumentando el riesgo en caso de que esta se encuentre detectable. Ambos virus infectan sitios anogenitales y están influenciados por los mismos factores de riesgo como ser número de parejas sexuales.
La concentración de citoquinas cervicovaginales aumenta el riesgo de adquirir VIH con aumento de otras infecciones de transmisión sexual (ITS) llevando a una alteración de la microbiota de la vagina con la depleción de Lactobacillus. Esto se debe a la interrupción de la barrera mucosa vaginal con aumento de proteasas de neutrófilos y aumento de CD4+ en el epitelio; principal zona de ataque del VIH. La acumulación de elementos inflamatorios requeridos con el fin de eliminar al HPV se asociaría a un aumento de la adquisición del HIV por lo mencionado con anterioridad. (Katharine J Looker, 2018)
El aumento de las células de Langerhans puede desempeñar un papel en la mejoría de la susceptibilidad del VIH al unirse a GP120 del HIV y facilitar la transmisión a las CD4+. La expresión de células natural Killer (NK) aumenta el riesgo de VIH.
La circuncisión y el TAR adecuado pueden reducir directa o indirectamente la adquisición de HPV y/o progresión de la enfermedad.
Es conocido que el virus del papiloma humano puede aumentar la susceptibilidad al VIH al romper la barreta epitelial reclutando células objetivo del HIV o generando un ambiente proinflamatorio lo que no se sabe es que si el aumento de adquisición del HIV está en relación estrecha con el tipo y/o diferentes genotipos de VPH o el tiempo de infección.
El riesgo de adquisición de HPV en contexto de HIV es el doble con una eliminación reducida hasta la mitad aumentando la persistencia con menor recuento de CD4+. (Katharine J Looker, 2018)
|
Efecto inmunológico |
Consecuencia clínica |
|
Disminución de CD4+ |
Mayor persistencia del HPV y progresión a HSIL |
|
Aumento de la carga viral VIH |
Asociación con mayor incidencia de lesiones de alto grado y cáncer invasor |
¿Cuál sería la interacción entre el HPV y VIH en el cáncer de cérvix?
La infección con VIH exacerba el riesgo de todos los canceres relacionados o no SIDA. El cáncer de cuello de útero es una condición definitoria del SIDA y es el más frecuente diagnosticado en la mujer con HIV.
Las mujeres que tienen sexo con mujeres (MSM) tienen mayor exposición del HPV con menor adherencia a la prevención y cribado. Las mujeres que viven con VIH son 6 veces más propensas a desarrollar cáncer de cérvix.
La adecuada TAR se asocia con disminución del cáncer de cérvix, pero no disminuye en un 100% el desarrollo de este.
Cabe destacar que la interacción entre VIH y HPV es compleja, multifactorial y bidireccional creando un sinergismo que acelera el proceso oncológico. (Pavone G., 2024)
Impacto de la Coinfección del HPV / VIH en la Inmunosupresión, Genotipo de HPV y Biomarcadores
Los CD4+ son esenciales para coordinar la inmunidad adaptativa mediando la respuesta inmune contra el HPV. El HIV, por su parte, ataca a las CD4+ provocando un descenso de estas lo que dificulta la eliminación del HPV generando persistencia y progresión.
La coinfección de HPV/HIV aumenta la desregulación de la expresión de oncogenes virales promoviendo la división celular y la inestabilidad genómica.
La inflamación crónica promueve el crecimiento de nuevas células, angiogénesis y remodelación de tejidos otorgando un microambiente apto para el cáncer.
El sistema inmunológico debilitado favorece la integración del HPV-AR en el genoma del huésped alterando la función de la célula normal y aumentando la progresión a neoplasia.
Mediante la PCR con genotipificación los HPV más presentes fueron: 16-18-31-33-35-58. Con respecto a los biomarcadores moleculares el más utilizado es la tinción dual (p16/Ki-67) que está asociado a mayor agresividad con un potencial metastásico. (Swase T.D, 2025)
El VIH tiene alta incidencia en Asia, Europa y América Latina con una presencia de genotipos variables según la región como, por ejemplo: Brasil: 16-56-70, Dinamarca:35- 51-52-58.
|
Recuento CD4+ |
Riesgo de HSIL |
|
>500 cell/mm³ |
Bajo |
|
200–500 cell/mm³ |
Moderato |
|
<200 cell/mm³ |
Alto |
Importancia del Papel de la Terapia Antirretroviral en el Tratamiento de la Lesión de la Lesión Precursora y Cäncer de Cérvix
Como se mencionó con anterioridad, aquella mujer con un bajo recuento de CD4 es propensa a la persistencia y progresión de enfermedad hacia la lesión intraepitelial con posterior desarrollo de patología maligna de cuello uterino en una velocidad más acelerada.
El inicio de la TARV logra un control virológico rápido y mantener la adherencia al tratamiento condujo a una mejor reconstitución inmune a nivel de las mucosas mejorando los resultados en la salud.
“En un metaanálisis que incluyo el análisis de 11 estudios, la estimación resumida de las lesiones cervicales incidentes fue menor en el WLHIV en la TARGA (0,81; IC del 95%: 0,60–1,08). La TARGA se relacionó con un menor riesgo de progresión de la lesión cervical (0,76; IC 95%: 0,64–0,92; I2 55,6%) y mayor tasa de regresión de estas lesiones (1,43, IC 95%: 1,06–1,94, I2 81%). Aunque la adquisición del VPH no fue significativamente menor en las usuarias de TARGA (0,83, IC del 95%: 0,40-1,70), el aclaramiento de la infección por el VPH fue mayor en el WLHIV en el tratamiento con TARGA (1,41; IC del 95%: 1,14-1,76; I2 2.4%). Concluyeron que la revisión proporciona evidencia de que la TARGA ayuda a reducir la incidencia y la progresión de las lesiones cervicales y a mejorar su regresión en las mujeres que viven con el VIH. Por lo tanto, se debe recomendar el régimen de TRAGA a todas las WLHIV con consejos para la adherencia a fin de permitir la reconstitución inmunitaria temprana”. (Ruchika Gupta, 2022)
“Otra revision en el 2005 de Harris y colaboradores busco determinar la incidencia de lesiones escamosas intraepiteliales (SIL) en mujeres seropositivas al VIH. eran mujeres estadounidenses seropositivas para el VIH (n = 855; edad media, 36 años) y seronegativas para el VIH (n = 343; edad media, 34 años) con citología cervical basal normal que se inscribieron en el Women's Interagency HIV Study (WIHS), un estudio de cohorte prospectivo multiinstitucional de gran tamaño. Desde su reclutamiento durante 1994-1995, los participantes de WIHS han sido seguidos semestralmente con pruebas de Papanicolaou repetidas durante una mediana de 7 años. La incidencia acumulada de cualquier SIL y SIL de alto grado o cáncer (HSIL+) se estimó de acuerdo con los resultados basales del ADN del VPH, estratificados por el estado serológico del VIH y el recuento de células T CD4. Concluyo que la baja incidencia acumulada similar de cualquier SIL entre las mujeres seronegativas y seropositivas para el VIH con recuentos de CD4 superiores a 500/microL y que tuvieron resultados normales en las pruebas de citología cervical y VPH negativos indica que las prácticas similares de detección del cáncer cervicouterino pueden ser aplicables a ambos grupos, aunque esta estrategia amerita una evaluación en un ensayo clínico apropiado.” (Tiffany G Harris, 2005)
En otro metaanálisis se extrajeron y revisaron un total de ochenta y cuatro (84) artículos de bases de datos electrónicas estándar, principalmente Web of Science, PubMed y Scopus. Los artículos se publicaron en inglés entre 2008 y 2024 y contaron con un total de 80023 participantes. revela una alta prevalencia de múltiples genotipos de VPH de alto riesgo entre las personas VIH positivas, lo que destaca el impacto de la coinfección por VPH y VIH en el desarrollo de cáncer de cuello uterino. Se encontró que los recuentos bajos de CD4, que van de inmunosupresión grave a moderada, se asocian con una mayor persistencia y progresión de las infecciones por VPH-AR, lo que enfatiza la necesidad de una atención eficiente del VPH/VIH para reducir la inmunosupresión. (Swase T.D, 2025)
Microbioma Vaginal, HPV Y VIH
La alteración de la microbiota vaginal favorece la coinfección de HIV y HPV.
Los Lactobacillus (spp.) producen ácido láctico, un potente microbicida que mantiene del pH ácido de la vagina; este microambiente es responsable de inactivar patógenos como el virus de inmunodeficiencia humana (VIH) y el virus del herpes simple (VHS) tipo 2, y al excluir anaerobios. En contraste, una microbiota vaginal es diversa, polimicrobiana y dominada por anaerobios, como Gardnerella vaginalis, Atopobium vaginae, Prevotella bivia, entre otros. Esta disbiosis, conocida como tipo de estado comunitario (CST) IVa (dominancia de G. vaginalis) y IVb (altamente diversa, sin ninguna especie particular), está fuertemente asociada con inflamación genital y daño epitelial. Muchos factores del huésped y externos influyen en la composición de la microbiota vaginal (MV) como ser la anticoncepción oral (estrógenos), la actividad y prácticas sexuales, el tabaquismo, la menstruación, el embarazo, la menopausia y el uso de antibióticos.
El papel de la MV en la adquisición del riesgo de VIH ha sido demostrado. Los estudios han mostrado que las comunidades microbianas vaginales alteradas, asociadas a la vaginosis bacteriana (BVAB), aumentan el riesgo de adquisición de VIH y modifican la eficacia de los microbicidas basados en antirretrovirales.
Los estudios han mostrado que las seropositivas tienen microbiotas vaginales no óptimas, que están asociadas con inflamación vaginal, excreción de VIH y un mayor riesgo de transmisión sexual a sus parejas. El impacto de la terapia antirretroviral (TAR) en la microbiota vaginal es actualmente desconocido, aunque la evidencia sugiere que el VIH aumenta la patogenicidad del VPH y tienen un mayor riesgo a cáncer cervicouterino, incluso aquellas bajo TAR.
Entender la interacción entre el VIH, el VPH de alto riesgo, la MV y la TAR es relevante y necesario para establecer políticas sobre programas de detección adecuados y manejo de las pacientes con VIH + para aliviar la carga del cáncer cervicouterino en esta población vulnerable.
Los cambios en la microbiota vaginal contribuyen al desarrollo de lesiones cervicales precoces debido a la inflamación crónica del cuello uterino conduce a desarrollo de como la enfermedad inflamatoria pélvica (EPI) y la vaginosis bacteriana (VB), ambas asociadas con infecciones persistentes por VPH y cáncer de cuello uterino.
En un estudio en el África subsahariana y en mujeres infectadas con VIH han demostrado que un cambio en la diversidad microbiana como resultado de la VB es detectable. Dado que se espera que las tasas de cáncer cervical aumenten en África subsahariana a medida que la población VIH-positiva reciba terapia antirretroviral (TAR) que prolonga la vida, es aún más importante entender los factores de riesgo asociados con el microbioma cervical.
Encontramos que el VPH estaba en alta abundancia en la cohorte los pacientes que eran positivos para VIH también fueron positivos para uno o más VPH. Entre las muestras de VIH, el VPH estaba asociado con al menos un aumento de 10 veces en Bacteroidetes y fusobacterias, así como una disminución en Actinobacteria.
Un desequilibrio en estas defensas puede resultar en cambios fisicoquímicos que producen alteraciones de la mucosa vaginal y del epitelio cervical. En este estudio, se demostró que el VIH tenía un efecto significativo en el microbioma cervical, aumentando la riqueza bacteriana y disminuyendo la diversidad beta. Estos resultados son similares a lo que se ha informado para el microbioma cervicovaginal y sugieren que los cambios en el microambiente del epitelio cervical provocados por el VIH ejercen una presión selectiva sobre las comunidades bacterianas cervicales (24–28). Mycoplasma fue significativamente más abundante en pacientes positivos para VIH. Se determino una fuerte asociación entre la gravedad de la infección por M. genitalium y la excreción de VIH desde el cérvix dejando en claro es que M. genitalium infecta los epitelios, rompiendo las uniones estrechas e induciendo una respuesta inflamatoria crónica. (Cameron Klein, 2019)
Sería deseable realizar futuros estudios que recluten una cohorte de todas las mujeres VIH-positivas con y sin lesiones cervicales para caracterizar mejor el microbiota asociado al VIH que promueve la infección por VPH y la progresión a cáncer cervical.
En otro estudio se exploró el impacto de la infección por VIH y VPH en la MV en pacientes con VIH, determinamos la prevalencia de la infección por VPH-AR y las anomalías citológicas cervicales en una cohorte de 44 seropositivas y 39 mujeres seronegativas (MSN), caracterizamos la microbiota vaginal mediante secuenciación de 16S. Se concluyo la predominancia de L. Iners en la VM, combinada con la alta prevalencia de HR-HPV tiene implicaciones clínicas potenciales tanto para las mujeres que viven con VIH como para las mujeres sin VIH. Por lo tanto, las mujeres seropositivas podrían beneficiarse de un seguimiento más cercano y podrían ser candidatas para intervenciones basadas en el microbioma. Se justifica realizar un trabajo adicional para entender las complejas interacciones entre el huésped, la VM y el HPV en mujeres coinfectadas con VIH y HR-HPV, incluyendo a WLWH en tratamiento antirretroviral (ART). (Monserrat Chávez-Torres, 2023)
Prevención Primaria: Vacunación en Pacientes VIH+
La OMS recomienda programas de vacunación dirigidos a niñas de 9 a 13 años, y los CDC recomiendan la vacunación rutinaria contra el VPH para niñas (y niños) de 11 a 12 años. Sobre la base de los datos de inmunogenicidad, la OMS y los CDC recomiendan esquemas de 2 dosis para aquellos menores de 15 años y esquemas de 3 dosis para aquellos de 15 años o más para todas las vacunas contra el VPH.
La prevención primaria es de suma importancia ya que las vacunas tienen una buena tasa de seroconversión en estos pacientes, aunque un poco más bajo que en pacientes no HIV+. Provoca una respuesta inmune protectora con disminución de verrugas y otros canceres. Se debe administrar en 3 dosis. La vacunación contra el VPH en personas que viven con VIH ha sido bien tolerada y segura.
Un estudio de Gardasil en niños que viven con VIH de 7 a 12 años informó una alta seroconversión, inmunidad específica del tipo de VPH persistente a 4 años y células de memoria inmunitaria, aumento significativo y persistencia de los títulos de anticuerpos después de un refuerzo adicional (cuarta dosis).
Otro estudio de Gardasil en hombres adultos que viven con VIH también encontró una alta seroconversión además de un buen perfil de seguridad.
Otro estudio reportó una tasa de seroconversión similar a la de Gardasil en mujeres que viven con VIH y mujeres HIV negativas de 13 a 27 años.
El Comité Asesor sobre Prácticas de Inmunización recomienda la vacunación contra el VPH en 3 dosis (en 0, 1 o 2 y 6 meses) para mujeres y hombres de 9 a 26 años que tengan condiciones de inmunocompromiso primarias o secundarias. (Castle P.E., 2021) (Fleider L, 2022)
En República Argentina el esquema de vacunación contra el VPH presenta el esquema de una única dosis será para las personas hasta los 20 años inclusive. El esquema será de dos dosis separadas por 6 meses para mayores de 21 años debido a el análisis de los estudios con respecto a la respuesta vacunal y de impacto de la estrategia, donde se evidenciaba un bajo porcentaje de aplicación de 2° dosis. La decisión de reducir nuevamente el número de dosis a un esquema de dosis única en los menores de 20 años, informada en diciembre de 2023, está avalada por la Comisión Nacional de Inmunizaciones (CoNaIn) y sigue las recomendaciones del grupo de expertos del Grupo de Expertos de Asesoramiento Estratégico (SAGE, por sus iniciales en inglés) sobre inmunización de la Organización Mundial de la Salud (OMS)
La edad límite de vacunación los 26 años inclusive para varones y mujeres (nacidas desde año 2000 y varones 2006). Sin embargo, se continuará con esquema de 3 dosis en la población de 11 a 26 años que viva con VIH, trasplantadas y/o que presente las siguientes condiciones: Lupus Eritematoso Sistémico (LES), Artritis Idiopática Juvenil (AIJ), Enfermedad Inflamatoria Intestinal (EII), Dermatomiositis (DM) y otras enfermedades autoinmunes en plan de recibir drogas inmunosupresoras. La secuencia de aplicación es de 0,1-2 y 6 meses (Argentina, 2024)
Prevención Secundaria: Cribado en Pacientes VIH +
La OMS recomienda el uso de pruebas de ADN del VPH como la prueba principal de detección de cáncer cervical, aunque las pruebas de Papanicolaou (PAP) deben continuar usándose según las pautas locales en varios entornos cuando las pruebas de ADN del VPH no están operativas. Estas pautas recomiendan la detección basada en pruebas del VPH para mujeres de 30 o más.
Para las mujeres que viven con VIH, estas pautas recomiendan la detección basada en pruebas del VPH para mujeres de 25 a 49 años cada 3. La Sociedad Americana de Oncología Clínica (ASCO) recomiendan que las mujeres que viven con VIH se sometan a una detección más temprana con un intervalo más corto utilizando pruebas del VPH en comparación con lo que se recomienda para las mujeres VIH-negativas y la población general dentro de la estratificación de recursos.
La asociación española de patología cervical y colposcopia recomienda que el cribado del CCU en mujeres que conviven con el VIH debe iniciarse a la edad de 25 años y mantenerse de por vida y debe realizarse mediante la prueba del ADN del VPH cada tres años. (Castle P.E., 2021)
En Argentina se recomienda inicio del tamizaje con citología a los 3 años del inicio de relaciones sexuales (IRS) para pacientes inmunocompetentes siguiendo el intervalo negativo 1-1-3 años. En cambio, en aquellas con inmunocompromiso como ser VIH+ se recomienda en inicio del tamizaje al año del IRS continuando sus controles anuales estrictos. (FASGO, 2022)
El Virus del Papiloma Humano (HPV) es una infección de transmisión sexual altamente prevalente, con más de 200 genotipos identificados. Entre ellos, aproximadamente 14 se consideran de alto riesgo oncogénico, responsables de la mayoría de los casos de cáncer de cuello uterino. El HPV tipo 16 es el más frecuentemente relacionado con lesiones precancerosas y cáncer invasor. La clasificación de las lesiones cervicales se basa entre lesiones de bajo y alto grado siendo esencial para el seguimiento clínico y la toma de decisiones terapéuticas. (FASGO, 2022)
Ciclo de Vida del HPV
Los virus del HPV son partículas virales dentro de 50-60 nm y carecen de envoltura lipídica. Es ADN doble cadena de 8 KP. empaquetado con histonas del hospedador y encapsulados por proteínas tardías codificadas por el virus. El genoma del HPV tiene 8 marcos de lectura abierto que se dividen en proteínas tempranas (E) y proteínas tardías (L) y una región reguladora de control. La proteína L1 y L2 codifican las proteínas para las cápsides.
L1: tiene regiones variables y constantes, las ultimas llevan los epítopos antigénicos específicos de la superficie que interactúan con la membrana basal del huésped al ingresar.
E1-E2: regulan el ciclo de vida viral y la replicación del genoma viral.
E4: regula los productos virales tempranos. Altera el citoesqueleto y facilita la eliminación de virones.
E5: aumenta la señal de crecimiento y la supervivencia dentro de la célula del huésped. Estimula la vía del Factor de crecimiento epidérmico (EGFR) favoreciendo un estado con tendencia a la malignidad.
E6-E7: causan desregulación del ciclo celular y actúan como oncoproteinas.
E6: unión y degradación de P53 inhibiendo la apoptosis estimulando a las células del HPV a sobrevivir y acumular daño genético. La proteína del HIV conocida como VPR modula la actividad de las moléculas que intervienen en la vía de P53 estimulando aún más la oncogénesis de E6.
E7: se une a la proteína del retinoblastoma (pRB) impulsando de manera apropiada la progresión del ciclo celular.
Después que la membrana basal se expone a un trauma, la proteína L1 se unía a proteoglicanos de sulfato de heparina (HSPGs) induciendo un cambio conformacional dependiente de ciclospilina B en la estructura de L1 exponiendo la porción N_terminal de la proteína menor de la cápside: L2. Una proteasa celular provoca la escisión por furina. La proteólisis de L2 es seguida por interacciones subsecuentes de L1 con HSPGs produciendo perdida de enlaces involucrados en la interacción inicial de L1 lo que provoca el movimiento viral al queratinocito y la exposición de residuos virales al comportamiento endocítico para internalizar al virus por endocitosis. La célula basal es reservorio. Una vez que esta el virus, el genoma viral se transporta al núcleo y queda en su forma episomal.
La infección se produce en un lapso de 12-24 hs, en la división basal: una célula queda y la otra célula sube. En la división celular, E2 une los genomas virales a los cromosomas mitóticos celulares, asegurando que queden envueltos en el núcleo y se dividan equivalentemente cada célula hija
E1-E2: complejo con ADN viral para reclutar ADN polimerasa del huésped.
L1 y L2 son sintetizadas y responsables del empaquetamiento del ADN viral y solo se expresan en los queratinocitos terminalmente diferenciados.
Durante la fase tardía de la infección, las células infectadas aumentan la expresión de las proteínas de la cápside que son altamente inmunogénicas. Los anticuerpos protectores contra el HPV surgen de 6 a 12 meses en caso de que se formen lo que sugiere que las células T controlan la replicación viral temprana.
Las pacientes con VIH+ con disminución de recuento de CD4+ presentan susceptibilidad al HPV, persistencia y desarrollo de cáncer. La paciente con lesión intraepitelial de alto grado (HSIL) tiene disminución de respuesta Th1 con estimulo de INF gamma e IL2 y tiene Th4 sesgado con el consiguiente aumento de Th17 con tendencia a la progresión.
La detección de aminoácidos virales por TLR9 (receptor) es importante en la respuesta inicial al HPV, estando aumentado en HPV de bajo riesgo (HPV-BR) y disminuido HPV-AR, posible mecanismo de bloqueo de la inmunidad innata.
En contexto de VIH+ la eficacia del sistema inmunológico disminuye aumentando el riesgo de transformación maligna y progresión por supresión inmunitaria con mayor tasa de recambio celular.
E7 recluta histona para bloquear a TLR9 y junto a E6 bloquea los receptores de reconocimiento de patógenos.
El HPV manipula la vía de señalización NF-KB y regula la cascada inflamatoria crónica aumentando aún más TRL9 sostenida sin respuesta antiviral estimulando más la inflamación crónica.
Ante el ataque viral, las células de Larghengans que residen en la epidermis migran a los órganos linfoides secundarios y preparan la inmunidad adaptativa. El HPV puede bloquear este paso.
La metilación del promotor mediada por E7 disminuye las células de Larghergans generando una reducción de las mismas con pobre activación de células T efectoras por lo cual CD8+ no actúan de manera correcta. Llevando a estado de inmunosupresión que está impulsado por indoleamina 2,3-Dioxigenasa (IDOI) incluye la generación de células T reguladoras o la supresión de la respuesta dependiente de la disminución de triptófano. El HPV aumenta IDOI con consiguiente disminución de triptófano. (Romaniya Zayats, 2022)
Interacción entre el HIPV y HPV para el Desarrollo del Cáncer de Cérvix
A. Disfunción del Sistema Inmunológico en la Coinfección de Ambos:
Es un tema difícil de entender. El VIH aumenta el riesgo de HSIL más aun con HPV-AR la persistencia de este último facilitada por la inmunosupresión del VIH se ha identificado como uno de los principales factores de riesgo para el desarrollo de HSIL; exacerbado por la disfunción de los Linfocitos T específicos para las oncoproteinas del HPV (inducido por VIH). Esta supresión inmunológica es más pronunciada en VIH+ avanzado con una deficiencia prologada y con mala adherencia al tratamiento antirretroviral.
El VIH ataca a las CD4+ llevando a la apoptosis y depleción celular. Los marcadores de la apoptosis de las células T CD4 como ser TRAIL, micropartículas, CCR5, TNRF2 aumentan la viremia por VIH. La disminución de CD4 conduce a un estado de inmunocompromiso. En los tejidos coinfectados existe un aumento de células dendríticas (CD) que expresan el marcador CD19 (fenotipo inmaduro) por disminución en la expresión de CD 83-86 evadiendo el ataque con HPV estimulando la persistencia. La CD no solo detecta al VIH-1 sino que también puede ser infectada por este transmitiendo la infección a las CD4+.
El captador especifico de CD sin integrar (DC-SING) en la superficie de las CD actúa como un receptor de patrones en el sitio de GP120 del HIV. Al iniciarse una respuesta adaptativa dependerá de la estructura de los N_glicanos en el patógeno de VIH-1, a mayor número de N_glicanos, mayor unión de VIH a DC-SING. Las células T activadas y las células presentadoras de antígenos aumentan por demás el complejo de histocompatibilidad II (HLA-DR) que promueve la coinfección de HPV/VIH generando una respuesta adaptativa inadecuada y tardía para la eliminación del HPV.
Las CD de los coinfectados pueden atenuar la función de las células T efectoras a través de señales inmune inhibitorias que involucran la vía PD-L1 conduciendo a la perdida de función de los linfocitos citotóxicos potenciado aún más por el VIH. además, las células tumorales cervicales pueden inhibir la migración de las CD a los ganglios linfáticos por disminución de CCR7 estimulando la producción de metaloproteinasa de matriz 9 (MMP-9) favoreciendo el ambiente tumoral.
Las CD plasmaticoides disminuyen en la infección por HIV dando lugar a infecciones oportunistas.
La disbiosis vaginal conduce a un estado proinflamatorio con supresión inmunitario otorgando un ambiente favorable para la persistencia de ambos virus.
B. Transición Epitelial y Mesenquimatosa en el Cáncer de Cérvix por la Coinfección:
El HIV por sus proteínas GP120 y TAT puede inducir la transición epitelio- mesénquima en el cérvix generando progresión de lesiones intraepiteliales. Es un proceso fisiológico que regula la diferenciación y adquisición de la identidad de la línea celular durante el desarrollo; sin embargo, facilita la progresión al promover el crecimiento y la metástasis dando que genera una pérdida de la polaridad apical basal, descomprime los viriones, disminuye marcadores y células de adhesión. Se encuentra regulado por el Factor transformante beta (TGF-b).
La proteína GP120 y TAT aumentan la invasión de células atípicas contribuyendo a la propagación de metástasis y resistencia al tratamiento.
El aumento de la transición epitelio-mesénquima (ETM) se encuentra favorecido por la disminución de E-cadherina y citoqueratina con el aumento de N-cadherina y vimentina. Además, estimula la vía Wnt/B-catenina.
La proteína TAT potencia la actividad transcripcional de E6 y E7. También induce a ETM en las células infectadas por HPV aumentando su invasidad mediado por vías de señalización como TGF-B y proteínas activadas por mitógenos (MAPK)
La proteína VPr interrumpe el control del punto del ciclo celular G2/M aumentando la acumulación de mutaciones en las células infectadas por el HPV exacerbando la malignidad.
Toda esta alteración del sistema inmunológico conlleva a una disminución en la vigilancia y eliminación del HPV pensando en un probable sinergismo molecular entre ambos virus.
El contacto entre las células de la mucosa oral y anogenital con el virus de la inmunodeficiencia y su interacción con GP120 y TAT conduce a disfunciones de las uniones ETM. La alteración de E-cadherina y CD44 está asociada con la severidad de lesiones intraepiteliales de cuello uterino. El VIH altera el perfil de citoquinas locales empeorando el curso natural de la infección por HPV. (Pavone G., 2024)
Los cofactores entre el VIH y las lesiones cervicales premalignas están dado por el inicio precoz relaciones sexuales, falta de métodos de barrera, múltiples parejas sexuales, antecedentes de infecciones de transmisión sexual (por ejemplo, infecciones por clamidia), educación, uso de anticonceptivos orales, multiparidad, tabaquismo y bajo índice de masa corporal
Las lesiones precursoras de cáncer de cuello de útero son las manifestaciones ginecológicas más importantes y comunes en las mujeres que viven con VIH.
En las mujeres seronegativas, las lesiones precancerosas de cuello uterino se curan en la gran mayoría de los casos tras su tratamiento. No obstante, las mujeres que viven con VIH presentan resultados menos satisfactorios y sobre todo altos índices de recurrencia de estas lesiones, relacionadas con el grado de inmunosupresión.
La progresión hacia el cáncer es alrededor 10 y 20 años a nivel general. Las mujeres seropositivas al VIH tienen tasas más altas y rápidas de progresión a carcinoma y tasas más bajas de regresión que las mujeres seronegativas al VIH. Esto se debe a una disminución en la vigilancia de células T en la infección por VIH, lo que permite la replicación del VPH, resultando en la persistencia de la infección por VPH, la acumulación de mutaciones en las células infectadas y la proliferación descontrolada de células atípicas.
Las mujeres con VIH han de realizarse revisiones con citología (Papanicolau) cada seis meses tras el diagnóstico y anualmente, una vez han obtenido dos resultados negativos consecutivos.
Las LIE de bajo grado rara vez progresan a LIE de alto grado o a cáncer cervical, aproximadamente el 10% de los pacientes, por ello no requieren tratamiento y el médico/a normalmente se limita a hacer un seguimiento de la lesión en las visitas semestrales por un lapso de dos años.
Las LIE de alto grado han de tratarse mediante la extirpación con asa diatérmica, láser o crioterapia. Estas técnicas son muy eficaces si se puede observar toda la lesión y la zona adyacente mediante colposcopia y si no existe afectación del canal cervical. En las mujeres que no cumplen estos criterios, la técnica de elección sigue siendo la conización cervical.
Se demostrado que la administración de TAR junto al tratamiento escisional reduce los índices de recurrencia de las LIE. Entre las mujeres que viven con VIH, una mayor cantidad de CD4, un tratamiento antirretroviral (TAR) antes del tratamiento y una carga viral de VIH más baja están asociadas con un menor riesgo de recurrencia.
Por lo cual es importante fomentar la meta de la OMS para el control del VIH de "90-90-90" (es decir, 90% diagnosticados, 90% tratados y 90% con carga viral suprimida) para el cuidado del VIH impactando de manera positiva en la consiguiente eliminación el cáncer cervical como un problema de salud pública a nivel mundial.
Materiales y Métodos
El presente estudio se realizó en el servicio de Ginecología del Hospital escuela de agudos Dr. Ramón Madariaga en la localidad de Posadas de la provincia de Misiones entre los periodos comprendidos desde el primero de enero de 2017 hasta el treinta y uno de diciembre del 2021, donde se recolectaron 2349 pacientes obtenidos de historias clínicas volcadas en una hoja de recolección de datos previamente elaborada y se recopilo la información clínica durante el periodo mencionado con anterioridad de las cuales 25 corresponde al universo estudiado el cual se expresa a través de tablas y gráficos estadísticos para cada una de las variables así como la combinación de los mismos para su interpretación y análisis.
Esta investigación es de tipo corte transversal, retrospectiva y descriptiva.
Criterios de selección:
- Criterios de inclusión
Pacientes de sexo femenino
Pacientes con diagnóstico de VIH
Pacientes con diagnóstico de lesiones intraepiteliales de cuello uterino - Criterios de exclusión
Pacientes de sexo masculino
Pacientes con diagnóstico de lesiones precursoras que no están infectados con VIH
Pacientes con diagnóstico de VIH que no padecen lesiones precursoras de cáncer de cuello de útero
Pacientes con diagnóstico de absceso cervical
Pacientes con diagnóstico de cáncer de cérvix
Variables:
Edad (Variable independiente cuantitativa numérica)
Tipo de lesión (Variable independiente cualitativa nominal)
Estado inmunológico (Variable independiente cualitativa categórica)
Carga viral (variable independiente cualitativa categórica)
Recuento de CD4+ (variable independiente cuantitativa numérica)
Tratamiento quirúrgico (Variable independiente cualitativa nominal)
Tratamiento antirretroviral (Variable independiente cualitativa nominal)
Relación entre el tipo de lesión intraepitelial y el recuento de CD4+ (Variable independiente cualitativa categórica)
Tiempo de evolución de la lesión precursora (Variable independiente cuantitativa categórica)
Seguimiento en conjunto (Variable independiente cualitativa categórica)
Nuevas lesiones (Variable independiente cualitativa categórica)
Consentimiento Informado: no se consideró necesario, dado que se trabajó con Historias Clínicas y el Servicio de Estadísticas suministró los números sin nombres para mantener el anonimato
Resultados
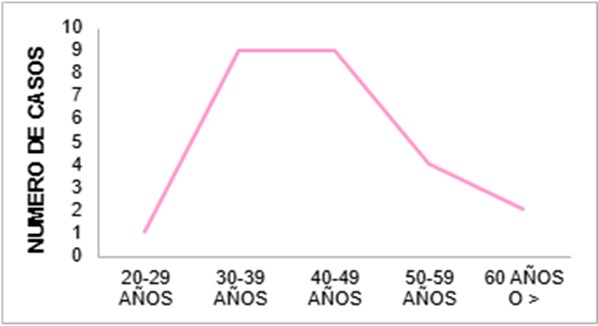
De las 2349 historias clínicas evaluadas en las cuales solo 25 pacientes cumplían con los criterios de inclusión, se puedo determinar que la edad promedio de diagnóstico fue alrededor de 43.28 años siendo el rango etario prevalente entre 30 a 49 años (18 pacientes), seguida por las de 50-59 años (4 pacientes), descendiendo de manera infrecuente en los extremos de la vida, es decir, en las mayores o igual a 60 años con un total de 2 y aquellas de 20 a 29 años solamente 1 paciente.
Edad
|
PROMEDIO |
43,28 |
|
EDAD |
N.º DE CASOS |
|
20-29 |
1 |
|
30-39 |
9 |
|
40-49 |
9 |
|
50-59 |
4 |
|
60 o MAS |
2 |
|
TOTAL |
25 |
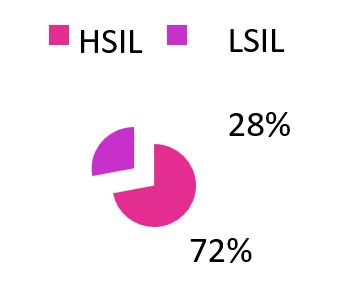
En cuanto al tipo de lesión intraepitelial se estableció una prevalencia de lesiones de alto grado (HSIL) en un 72% que correspondería a 18 casos contra un 28% correspondiente a Lesiones de Bajo Grado (LSIL) (7casos).
|
TIPO DE LESION |
N.º DE CASOS |
|
HSIL |
18 |
|
LSIL |
7 |
|
TOTAL |
25 |
Tipo de Lesión
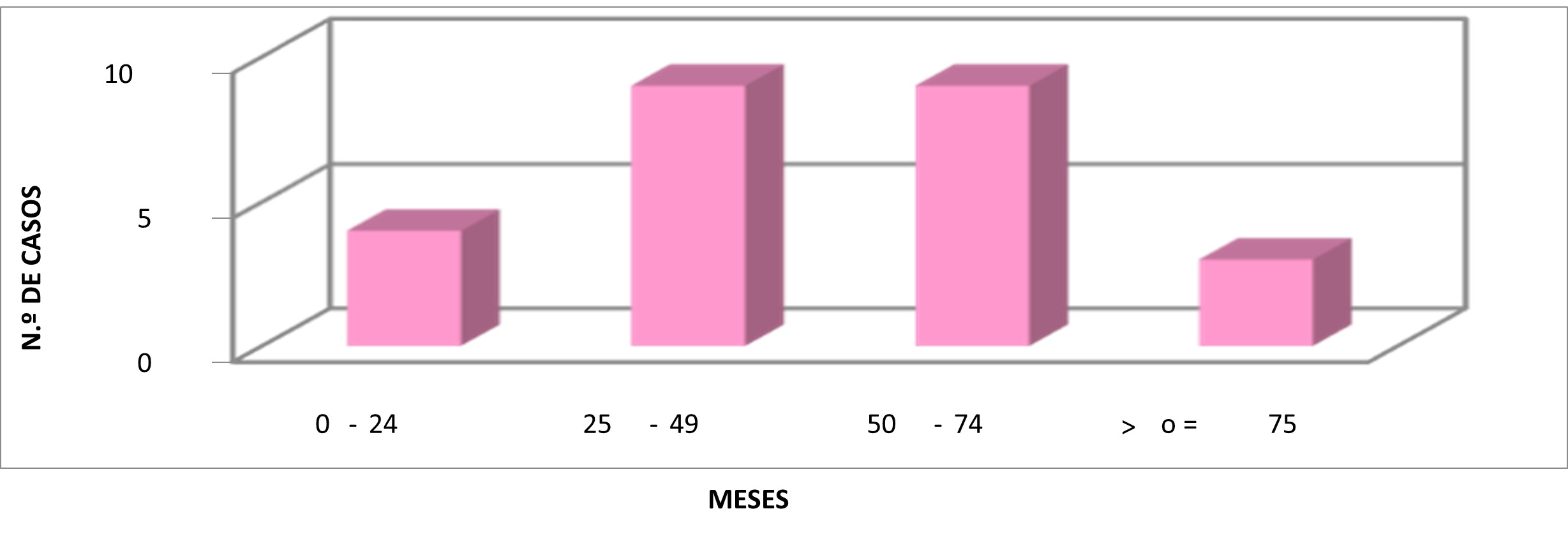
En lo que respecta al tiempo de evolución en la aparición de las lesiones precursoras, el promedio fue de 55,4 meses. Siendo apreciables en aquellas mayores a 2 a 4 años de diagnóstico de VIH. Siendo de evolución más rápida en aquellas menores a 2 años del diagnóstico, pero se vio fuertemente asociada al no cumplimiento del tratamiento antirretroviral o al abandono de este. De manera infrecuente solo en 3 pacientes con tratamiento crónico de más de 9 años se vio una evolución de la enfermedad asociada al abandono de la medicación y escaso seguimiento de su estado inmunológico.
|
PROMEDIO |
55,4 |
|
EVOLUCION EN MESES |
|
|
MESES |
N.º DECASOS |
|
0-24 |
4 |
|
25-49 |
9 |
|
50-74 |
9 |
|
> o = 75 |
3 |
|
TOTAL |
25 |
Tiempo de Evolución
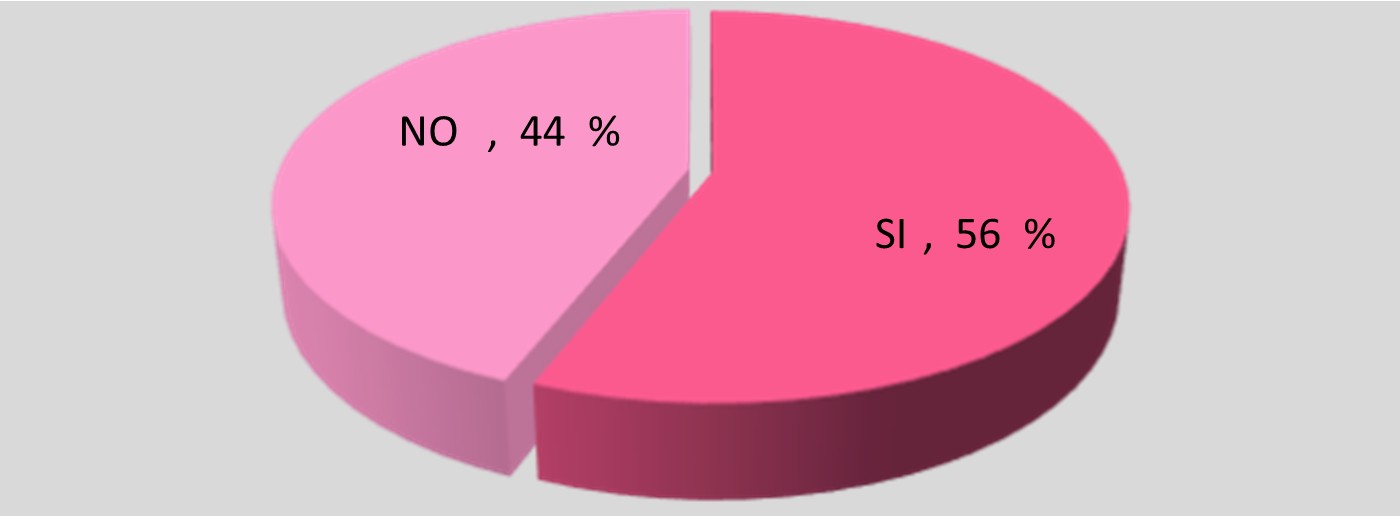
Teniendo en cuenta la realización de tratamiento quirúrgico, es decir conización cervical, se pudo realizar dicho acto quirúrgico en un 64% de los casos; 16 pacientes. El 36% (9 pacientes) no realizo tratamiento quirúrgico debido al ausentismo en el seguimiento en conjunto por parte de la paciente, abandono de medicación, negación de la enfermedad hasta el fallecimiento como se produjo en 5 pacientes. Con respecto al tratamiento elegido, no estaba protocolizado en aquel entonces como normativa de servicio la realización de escisión de la zona de transformación (LLETZ) y/o PEF en lesiones de bajo grado.
|
CONIZACION |
N.º DE CASOS |
|
SI |
16 |
|
NO |
9 |
|
TOTAL |
25 |
Tratamiento Quirúrgico
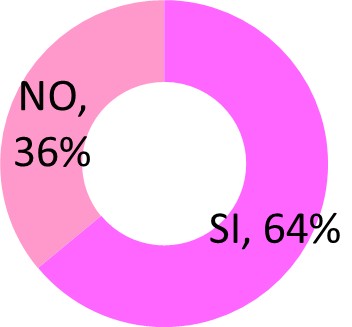
Una de las variables a estudiar fue el cumplimiento del tratamiento antirretroviral donde llama la atención la coincidencia con el tratamiento quirúrgico. Siendo un 64% que cumplió con tratamiento antirretroviral y realizó conización cervical contra un 36% que no realiza tratamiento, o lo hizo de manera inadecuada y tampoco realizó tratamiento quirúrgico.
|
TRATAMIENTO ARV |
|
|
SI |
16 |
|
NO |
9 |
|
TOTAL |
25 |
Tratamiento Antirretroviral

Debido al porcentaje significativo de pacientes que no realizaron tratamiento de forma adecuada surgió el interés de investigar el estado inmunológico de las 25 pacientes, se estableció que aquellas que no cumplían con el tratamiento antirretroviral, se encontraban inmunocomprometidas (9 pacientes), a diferencia de las que sí lo hacían, que se hallaban inmunocompetentes (16 pacientes).
|
ESTADO INMUNOLOGICO |
|
|
INMUNOCOMPETENTE |
16 |
|
INMUNOCOMPROMETIDA |
9 |
|
TOTAL |
25 |
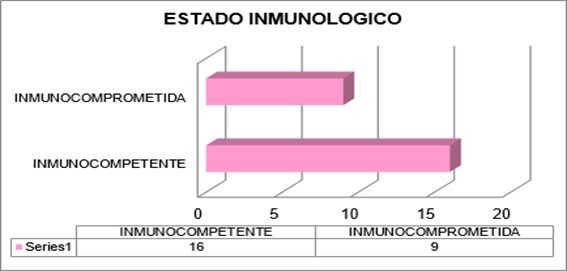
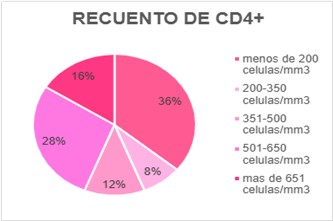
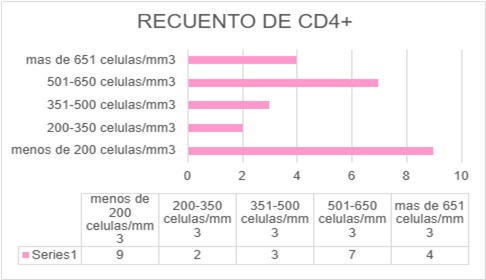
El estado inmunológico de las pacientes nos estimuló a profundizar en lo que respecta al recuento de CD4+ y carga viral donde pudimos observar el 36% (9/25) de las pacientes se encontraban en fase SIDA con carga viral detectable con mala adherencia o ausencia de tratamiento AR. Más del 44% (11/25) de las pacientes estudiadas presentaban CD4 > 500 cell/mm3 con una CV indetectable. En un 20% (5/25) las pacientes VIH presentaban un recuento de CD4+ entre 200 y 500 cell/mm3 con carga viral indetectable, esto podría deberse por el diagnostico e inicio de terapia antirretroviral en un lapso menor a 2 años.
Recuento de CD4
|
RECUENTO DE CD4 |
|
|
menos de 200 células/mm3 |
9 |
|
200-350 células/mm3 |
2 |
|
351-500 células/mm3 |
3 |
|
501-650 células/mm3 |
7 |
|
más de 651 células/mm3 |
4 |
|
TOTAL |
25 |
Carga Viral
|
CARGA VIRAL |
|
|
DETECTABLE |
9 |
|
INDECTECTABLE |
16 |
|
TOTAL |
25 |
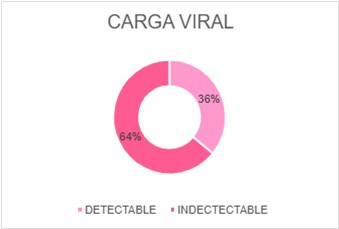
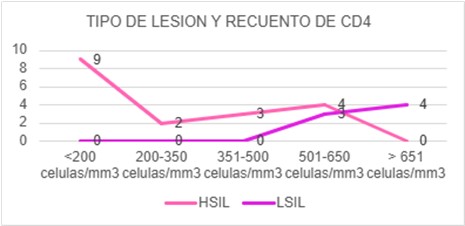
Esto nos estimuló aún más a determinar una asociación entre el tipo de lesión con el recuento de CD4 al momento diagnóstico. Pudiendo determinar cómo se ve en el grafico de línea que a mayor recuento de CD4, aumenta la proporción de LSIL y disminuye la de HSIL y viceversa.
|
RECUENTO DE CD4 |
HSIL |
LSIL |
|
<200 celulas/mm3 |
9 |
0 |
|
200-350 celulas/mm3 |
2 |
0 |
|
351-500 celulas/mm3 |
3 |
0 |
|
501-650 celulas/mm3 |
4 |
3 |
|
> 651 celulas/mm3 |
0 |
4 |
Al ser una enfermedad crónica surgió el motivo de investigar sobre el seguimiento en conjunto tanto en ginecología e infectología y se logró establecer que en el largo trayecto la paciente termina abandonando su seguimiento en algún momento de su vida.
|
SEGUIMIENTO EN CONJUNTO |
|
|
SI |
14 |
|
NO |
11 |
|
TOTAL |
25 |
Seguimiento en Conjunto
Este abandono por parte del paciente impacta desfavorablemente en la evaluación de la aparición de nuevas lesiones precursoras de cáncer de cuello uterino debido a que solo en una paciente se pudo demostrar la presencia de una lesión de bajo grado, a la cual ya se le había realizado una conización cervical, si bien presentaba una carga viral indetectable, el recuento de CD4+ era de 201 cell/mm3. En un poco más del 50% (13) no presentaron nuevas lesiones y, muy lamentable, en menos del 50% no se pudo determinar dicha variable debido a la falta y ausencia de control por parte de la paciente.
|
NUEVAS LESIONES |
|
|
NO |
13 |
|
SI |
1 |
|
NO SE SABE |
11 |
|
TOTAL |
25 |

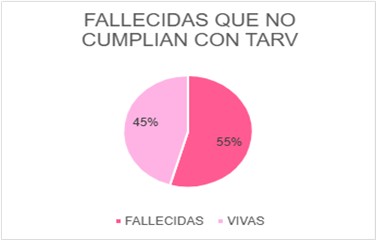
La falta de tratamiento antirretroviral por parte de las pacientes además del impacto negativo y la adquisición de enfermedades oportunista tuvo un desenlace fatal en 5 de las 9 pacientes correspondiente a un 55%.Esto evidencia de manera contundente la importancia de la adherencia al tratamiento y del control inmunológico.
|
FALLECIDAS DE LAS QUE NO CUMPLIAN CON TARV |
|
|
FALLECIDAS |
5 |
|
VIVAS |
4 |
Conclusiones
Debido a que el VPH y el VIH tienen muchas similitudes en cuánto a factores de riesgo y ruta de entrada, la coinfección es esperable. Se sabe bien que la inmunosupresión por VIH desempeña un papel fundamental en el establecimiento del VPH en el cuello uterino, lo que resulta en una mayor persistencia del VPH, así como un mayor riesgo de progresión a lesiones de alto grado, recurrencia y refractariedad al tratamiento en pacientes coinfectados.
La principal limitación de este estudio fue el número de la muestra. Como se trata de un estudio retrospectivo, hubo una brecha en el seguimiento de las pacientes para determinar si hubo recurrencia o no de lesiones. Solo en aquellas con terapia antirretroviral y seguimiento multidisciplinario se obtuvo información completa. En este trabajo observamos que las pacientes VIH + están estrechamente relacionada con una mayor persistencia de infección por VPH debido al compromiso inmunológico, como lo demuestra la proteína tat del VIH que promueve la progresión del ciclo celular y reduce la expresión de los inhibidores del ciclo celular. La infección por VIH induce un estado de inmunosupresión disminuyendo los niveles de linfocitos CD4+ y afecta la activación de las células dendríticas y la actividad de los linfocitos CD8+,quienes son clave en la eliminación de células epiteliales infectadas por HPV. Por lo tanto, la actividad del VIH contra los linfocitos CD4+ y CD8+ podría disminuir la eliminación de células epiteliales infectadas por HPV y promoviendo la desregulación del ciclo celular favoreciendo la persistencia.
El presente trabajo fue motivado por el incremento de casos de HIV en los últimos años y se puede apreciar que son más frecuente las lesiones de alto grado con respecto a las de bajo grado en pacientes con diagnóstico de VIH. Se puede ver reflejado en el mismo, que las que no cumplen con el seguimiento tanto infectológico como ginecológico tienen mala evolución, complicaciones e incluso el deceso de estas.
Con respecto a las pacientes con buen estado inmunológico, tratamiento adecuado y seguimiento correcto, se observó que el desarrollo de nuevas lesiones es muy infrecuente. De igual forma debido a la falta de seguimiento en algunas pacientes esto puede ser un sesgo.
Entonces se pudo concluir que aquellas con diagnóstico de VIH, inmunocompetentes, y cumpliendo el tratamiento antirretroviral y quirúrgico, y el no abandono del seguimiento tiene el mismo impacto que aquella paciente sin infección por VIH en el desarrollo de lesiones precursoras de cuello uterino. En cambio, cuando el recuento de células CD4 es bajo, cuando no están usando la terapia antirretroviral y tienen carga viral detectable; aumenta el riesgo de lesiones precursoras de cáncer de cuello uterino y de hasta fallecer por infecciones oportunistas. Por lo cual, el tratamiento y la atención óptima y precoz de los pacientes con VIH + es esencial para reducir la prevalencia de LIE y cáncer de cuello de uterino.
PROPUESTA
Brindar más información sobre educación sexual, para prevenir infecciones de transmisión sexual, y en caso de que se produzca la infección realizar un diagnóstico precoz, realizando serologías anuales a todas las pacientes sexualmente activas.
Búsqueda de otras ITS que puedan fomentar la disbiosis a nivel cérvico vaginal generando un estado proinflamatorio apto para la coinfección VIH/HPV.
Intensificar la educación a las pacientes sobre screening cervicouterino, de esta manera se podrá acceder al diagnóstico oportuno de lesiones precursoras.
Apoyo y manejo multidisciplinario de estas pacientes favoreciendo y estimulando el seguimiento de pacientes con dichas patologías para evitar la discontinuidad de tratamiento.
BIBLIOGRAFIA
- Alexandre Pérez-González, E. C. (2022). Update on the Epidemiological Features and Clinical Implications of Human Papillomavirus Infection (HPV) and Human Immunodeficiency Virus (HIV) Coinfection . Microorganisms.
- Argentina, M. d. (2024). Vacuna contra el Virus del Papiloma Humano (VPH) | 2024. En D. d. Inmunoprevenibles, Esquema de unica dosis de vacuna nonavalente (pág. 33). Republica Argentina.
- Bekana K. Tadese, X. Y.‐T. (2025). The Burden of HPV Infections and HPV‐Related Diseases Among People With HIV: A systematic Literature Review. Journal of Medical Virology.
- Cameron Klein, a. D. (2019). Relationship between the Cervical Microbiome, HIV Status and Precancerous Lesions. American Society for Microbiology.
- Castle P.E., E. M. (2021). Cervical Cancer Prevention and Control in Women Living . Division of Cancer Prevention, National Institutes of Health.
- CDC. (ENERO de 2025). https://www.cdc.gov/hiv/about/index.html. Obtenido de https://www.cdc.gov/.
- Delgado, R. (2011). Enfermedades Infecciosas y microbiologia Clinica. Elservier, 8.
- FASGO, S. S. (2022). Prevención primaria y secundaria del cáncer cervicouterino: “Manejo del tamizaje anormal y de las lesiones histológicas del cuello uterino”. En S. SOGIBA, Manejo del tamizaje anormal y de las lesiones histológicas del cuello uterino”. Argentina.
- Fleider L, P. C. (2022). Vaccination against HPV in Women and Men over 40 years of age. AAMA TGI Commission.
- Katharine J Looker, M. M.-C. (2018). Evidence of synergistic relationships between HIV and Human Papillomavirus(HPV): systematic reviews and meta-analyses of longitudinal studies of HPV acquisition and clearance by HIV. Journal of the International AIDS Society.
- Monserrat Chávez-Torres, M. G.-P.-S.-T.-R.-M.-C. (2023). The vaginal microbiota of women living with HIV on suppressive antiretroviral therapy and its relation to high-risk human papillomavirus infectio. BMC Microbiology .
- Pavone G., M. A. (2024). Entangled Connections: HIV and HPV Interplay in Cervical Cancer—A Comprehensive Review. International Journal of Molecular Sciences.
- Romaniya Zayats, T. T. (2022). HPV and the Risk of HIV Acquisition in Women. Frontiers in Cellular and Infection Microbiology.
- Ruchika Gupta, L. C. (2022). Terapia antirretroviral de gran actividad (TARGA) y desenlace de las lesiones cervicales y el VPH de alto riesgo en mujeres que viven con el VIH (WLHIV): una revisión sistemática y metanálisis. European Journal of Obstetrics & Gynecology and Reproductive Biology.
- Simona Claudia Cambrea, M. A. (2022). HPV and HIV Coinfection in Women from a Southeast Region of Romania—PICOPIV Study. PICOPIV Study.
- Swase T.D, F. I. (2025). The impact of HPV/HIV co-infection on immunosuppression, HPV genotype, and cervical cancer biomarkers. BMC Cancer.
- Tiffany G Harris, R. D. (2005). Incidence of cervical squamous intraepithelial lesions associated with HIV serostatus, CD4 cell counts, and human papillomavirus test results. JAMA.
-
Carrera Médico Especialista en patología TGI y colposcopia. Facultad de Medicina UBA.
Hospital Escuela de Agudos Dr. Ramon Madariaga (HEARM).
Grupo Oroño de Rosario.
Hospital de Clínicas San José de San Martín
