Evaluación de la Variación de los Síntomas más Frecuentes en la Perimenopausia y Posmenopausia con el Uso de Testosterona
Autores:
Báez Gabriel1, Britez Juliana1, Fochesatto Noelia2, Kule Alicia2, Kachuk Mariela3, Wimer Pamela4
Resumen:
Objetivo: Evaluar la variación en los síntomas como pérdida del deseo sexual, fatiga, dificultad para concentrarse y sentimiento de tristeza en mujeres perimenopáusicas y postmenopáusicas tratadas con testosterona tópica al 0,5% durante seis meses.
Pacientes y método: Un estudio de cohortes prospectivo llevado a cabo en mujeres perimenopáusicas y postmenopáusicas atendidas en un consultorio de ginecología entre los meses de diciembre del 2024 a mayo del 2025. 60 mujeres que fueron tratadas con gel de testosterona durante 6 meses con presencia de al menos uno de los siguientes síntomas: cansancio o fatiga, dificultad para concentrarse, sentimiento de tristeza y disminución del deseo sexual. Para medir la frecuencia y gravedad de los síntomas iniciales al uso de testosterona y luego de 6 meses de iniciar el tratamiento, se usó una versión modificada de la Escala Climatérica de Greene. Resultados: los cuatros síntomas estudiados mejoraron de forma significativa (p< 0.001) durante el período estudiado. El estado de ánimo mejoró más que la cognición (79% de mujeres indicaron una mejora en el estado de ánimo frente al 70% que informaron una mejora de los síntomas cognitivos). En cuanto a la pérdida de interés en el sexo, el 81% de las mujeres informaron una mejora. Conclusión: E l u s o de testosterona transdérmica durante 6 meses se asoció con mejoras significativas en el estado de ánimo y la cognición. Se necesita más investigación, incluidos ensayos clínicos aleatorizados, para establecer la eficacia y seguridad a largo plazo de la testosterona para el tratamiento de éstos y otros síntomas. Citas Bibliográficas: 10
Abstract
Objective: To evaluate the variation in symptoms such as loss of sexual desire, fatigue, difficulty concentrating, and feelings of sadness in perimenopausal and postmenopausal women treated with topical 0.5% testosterone for six months.
Patients and method: A prospective cohort study was conducted in perimenopausal and postmenopausal women seen in a gynecology clinic between December 2024 and May 2025. Sixty women were treated with testosterone gel for six months and had at least one of the following symptoms: tiredness or fatigue, difficulty concentrating, feelings of sadness, and decreased sexual desire. A modified version of the Greene Climacteric Scale was used to measure the frequency and severity of symptoms at baseline with testosterone use and six months after starting treatment. Results: All four symptoms studied improved significantly (p < 0.001) during the study period. Mood improved more than cognition (79% of women reported improved mood vs. 70% who reported improved cognitive symptoms). Regarding loss of interest in sex, 81% of women reported improvement. Conclusion: Use of transdermal testosterone for 6 months was associated with significant improvements in mood and cognition. Further research, including randomized clinical trials, is needed to establish the long-term efficacy and safety of testosterone for the treatment of these and other symptoms. Citas Bibliográficas: 10
Introducción
La perimenopausia y la menopausia es una etapa en la vida reproductiva femenina caracterizada por fluctuaciones hormonales, particularmente en los niveles de estrógenos y andrógenos. Estos cambios pueden generar sintomatología variada, entre la que se destacan la disminución del deseo sexual, la fatiga crónica, dificultad para concentrarse (1), trastornos del sueño, alteración del bienestar general, bajo estado de ánimo (2) y la dificultad para el descenso de peso. Estas manifestaciones comprometen la calidad de vida y generan un impacto clínico y emocional significativo.
En las mujeres, los niveles de testosterona circulante disminuyen con la edad y son hasta un 50% más bajos en mujeres menopáusicas en comparación con mujeres adultas más jóvenes (3), lo que probablemente contribuye a síntomas como la confusión mental y el estado de ánimo deprimido en la mediana edad.
Cabe destacar que la Declaración de Posición del Consenso Global en cuanto al uso de testosterona para mujeres, publica recientemente, y en simultáneo en 4 revistas, con sus respectivos autores representando a 10 sociedades, incluyendo la Sociedad Internacional para el Estudio de la Salud Sexual de la Mujer (ISSWSH) y respaldada por la ISSWSH conjuntamente con otras 10 sociedades de medicina sexual, endocrinología, obstetricia y ginecología, como también sociedades de menopausia. Ésta proporcionó orientación clínica sobre el uso de la terapia de testosterona en mujeres, examinando el efecto en la función sexual (6); bienestar, estado de ánimo y cognición; efectos musculoesqueléticos; salud cardiovascular y de los senos; así como efectos secundarios androgénicos y eventos adversos. Las conclusiones se desarrollaron basándose en la revisión sistemática y meta-análisis de los beneficios y riesgos de la testosterona terapia en mujeres, (5) y las recomendaciones de práctica clínica se basaron en la opinión de expertos y el consenso de los panelistas.
Según la Declaración de Posición Global, la única indicación basada en evidencia para la terapia de testosterona es HSDD en mujeres posmenopáusicas, utilizando un modelo biopsicosocial de evaluación y tratamiento. (6 y 7).
Un metaanálisis reciente concluyó que hay insuficiencia en evidencias de ensayos clínicos aleatorizados (ECA) para apoyar el uso de testosterona para tratar cualquier síntoma menopáusico que no sea la baja libido (8). En consecuencia, las pautas actuales solo recomiendan testosterona para tratar el bajo deseo sexual en mujeres menopáusicas, si la TRH por sí sola no es efectiva (9). Sin embargo, a menudo se prescribe testosterona a las mujeres en la práctica clínica porque los datos disponibles y la justificación fisiológica sugieren un beneficio general.
Objetivos:
El objetivo de este estudio fue evaluar el efecto de la testosterona 0,5% en gel durante el uso por 6 meses, sobre los síntomas como dificultad para concentrarse, en el estado de ánimo negativo, cansancio o fatiga persistente y pérdida de interés en el sexo, en mujeres perimenopáusicas y posmenopáusicas con síntomas persistentes sin el uso de la TRH estándar (estrógeno con o sin progesterona). Evaluamos sólo mujeres que usan testosterona transdérmica porque, en comparación con otras formulaciones de testosterona (oral, intramuscular y pellets subcutáneos), la testosterona transdérmica no está asociada con un mayor riesgo de eventos adversos graves cuando se usa en dosis fisiológicas (es decir, dosis que se aproximan a las concentraciones fisiológicas de testosterona en mujeres perimenopáusicas) (10). Los efectos secundarios como el acné y el crecimiento localizado de vello en el sitio de aplicación suelen ser leves, fácilmente reversibles con ésta vía de administración (eliminación de la aplicación).
Diseño Metodológico
Este fue un estudio de cohorte prospectivo de un solo centro de salud. (Hospital Nuestra Señora de Fátima).
Paciente (Material)
Se incluyeron mujeres que asistieron al Servicio de Ginecología entre el 1 de diciembre del 2024 al 31 de mayo de 2025 y que consultaron por sintomatología compatible con déficit androgénico y cumplieron criterios clínicos de perimenopausia y postmenopausia. Se contó con la aprobación del comité de ética.
Criterios de inclusión
- Mujeres entre 42 y 65 años.
- Diagnóstico de perimenopausia y postmenopausia basado en irregularidad menstrual, alteraciones del sueño, cambios de humor o síntomas vasomotores.
- Presencia de al menos uno de los siguientes síntomas: fatiga crónica, disminución del deseo sexual, sentimiento de tristeza o dificultad para concentrase.
- Habían completado un cuestionario de síntomas de menopausia (MSQ) antes de la iniciación de la testosterona, habían sido atendidas por el equipo multidisciplinario del Hospital en cuestión y habían completado el mismo MSQ seis meses después de iniciar la terapia de testosterona.
- No usaban simultáneamente otra TRH, no tomaron durante el periodo de estudio medicación antidepresiva.
- Firma del consentimiento informado, para que sus datos fueran utilizados con fines de auditoría.
- Pacientes con Índice de masa corporal menor a
- Todas las pacientes estudiadas debían tener realizado los siguientes controles ginecológicos anuales: examen clínico-ginecológico presencial, control de signos vitales peso y talla, ecografía ginecológica TV y mamaria, papanicolaou y colposcopía, laboratorio y mamografía.
Criterios de exclusión
- Diagnóstico actual o previo de hipotiroidismo no tratado o con tratamiento
- Patologías psiquiátricas severas (ej.: depresión mayor, trastorno bipolar, esquizofrenia).
- Evidencia clínica o bioquímica de
- Historia de cánceres hormono-dependientes (mama, endometrio).
- Terapia hormonal (testosterona, estrógenos, tibolona) en los 6 meses
- Enfermedad hepática activa o insuficiencia hepática
- Insuficiencia renal crónica estadio 4 o
- Historia de eventos tromboembólicos.
- Otras comorbilidades que contraindiquen el tratamiento o interfieran con la evaluación de resultados, según criterio médico.
Métodos
La Escala Climática de Greene es un cuestionario de 21 ítems que mide el número y la gravedad de los síntomas menopáusicos y ha sido validado para su uso en diferentes poblaciones (Greene 1998) (Anexo 1).
Todos los pacientes que son atendidos en nuestro Hospital por el equipo multidisciplinario bajo un programa que llamamos “Mujer activa” (Anexo 2), completaron el MSQ (cuestionario de síntomas de menopausia) una versión modificada de la Escala Climatérica de Greene (GCS) (Greene 1976) (Anexo 3).
Los pacientes califican la gravedad de cada síntoma utilizando una escala de Likert de 4 puntos, de 0 a 3, en donde 0 es “nada”- 1 es “un poco”-2 es “bastante”-3 es” extremadamente”.
El MSQ incluye 10 de los 21 síntomas enumerados en el GCS original.
Éste mismo MSQ es realizado por las pacientes, que usan testosterona transdérmica en nuestro hospital, a los 6 meses de tratamiento para evaluar la continuación del mismo tratamiento en caso de que hubieran experimentado beneficios significativos.
El enfoque del estudio fue evaluar el impacto del uso de testosterona, en 4 síntomas específicos, relacionados con la cognición (cansancio o fatiga, dificultad para concentrarse) y con el estado de ánimo (sentimientos de depresión o tristeza, disminución en la libido), al inicio luego de 6 meses de uso de testosterona (4 elementos).
Los pacientes fueron tratados con una única formulación magistral de testosterona 0,5% gel, jeringas prellenadas. (Anexo 4).
Resultados
Los datos fueron recolectados mediante el cuestionario de Greene aplicado en formato papel y cargados manualmente en una planilla de Microsoft Excel (versión 2007) para su procesamiento.
El análisis estadístico fue realizado con el apoyo del modelo de lenguaje ChatGPT (OpenAI), utilizado como herramienta de asistencia en el cálculo e interpretación de los datos. Todos los resultados fueron verificados posteriormente en Excel.
Se calcularon medidas de tendencia central (media), de dispersión (desviación estándar) y proporciones para describir las variables.
Para la comparación de las puntuaciones antes y después de la intervención se utilizó la prueba t de Student para muestras pareadas.
La comparación de la prevalencia de síntomas antes y después del tratamiento se realizó mediante la prueba de McNemar.
Se consideró un valor de p < 0,05 como estadísticamente significativo prueba t de muestras relacionadas (o pareadas).
Todos los pacientes fueron incluidos en el análisis basal para la prevalencia de síntomas. Por síntoma, solo se incluyeron pacientes que puntuaron 1, 2 o 3 antes de comenzar la testosterona al analizar el porcentaje de mujeres que informaron mejora de síntomas y el cambio en la puntuación de gravedad de síntomas a los 6 meses. Los pacientes que asignaron una puntuación de 0 a un síntoma en el análisis basal fueron excluidos del análisis a los 6 meses para ese síntoma individual. Por ejemplo, una paciente que puntuó ‘cansancio o fatiga’ con un 1, 2 o 3 en el análisis basal fue incluida en el análisis a los 6 meses para el cambio en la puntuación de síntomas de ‘cansancio o fatiga’; pero si la misma paciente puntuó ‘depresión o tristeza’ con un 0 en el análisis basal, no fue incluida en el análisis a los 6 meses para el cambio en la puntuación de síntomas de ‘depresión o tristeza’.
Se estudiaron los MSQ de 60 (n=60) mujeres que presentaban algunos de los síntomas estudiados. Éste MSQ fue realizado al inicio de cada tratamiento y a los 6 meses del mismo. La edad media fue (53.5 años). Ninguna mujer recibía otra terapia hormonal de reemplazo.
El tiempo medio tratamiento con testosterona hasta la realización del MSQ post tratamiento fue de 180 ± 20.4 días.
La prevalencia de síntomas en el análisis basal, y el número (%) de pacientes cuyos puntajes de síntomas mejoraron después de iniciar la terapia de testosterona se presentan en las Tablas 1 y 2, y en la Fig. 1.
Los síntomas estado de ánimo se informaron con más frecuencia que los síntomas cognitivos en el análisis inicial (prevalencia media 79%, rango 80–90%, frente a 70%, rango 75–78%, respectivamente; Tabla 1). La “pérdida de interés en el sexo” fue el síntoma basal más prevalente. El 90% de las mujeres informaron una libido reducida.
Los 4 síntomas mejoraron significativamente cuatro meses después de iniciar laterpaia con testosterona (tabla1). El 70% (rango 62–78%) de las mujeres con síntomas cognitivos informaron una mejora frente al 79% (rango 77–81%) de las mujeres con síntomas del estado de ánimo. Los dos síntomas más propensos a mejorar fueron ‘pérdida de interés en el sexo’ (el 81% de las mujeres informaron una mejora, p < 0.05) y ‘dificultad para concentrarse (78% de las mujeres, p < 0.05). ‘Cansancio o fatiga’ fue el menos reportado como mejora (62%).
Tabla 1: El número (%) de pacientes que informaron síntomas en la línea de base, y el número (%) de pacientes que informaron una mejora (una reducción en la puntuaciónde3a2,1o0;2a1o0,o1a0,después de6mesesdelusodeTestosterona.
|
Prevalencia de los síntomas en la línea base (n=60) |
Porcentaje de pacientes que reportaron mejoría de síntomas a los 6 meses |
||||
|
Síntomas cognitivos |
n |
% |
n |
% |
p |
|
Cansancio o Fatiga |
47 |
78 |
29 |
62 |
<0,05 |
|
Dificultad para concentrarse |
45 |
75 |
35 |
78 |
<0,05 |
|
Síntomas de estado de ánimo |
<0,05 |
||||
|
Sentimiento de depresión, tristeza |
48 |
80 |
37 |
77 |
<0,05 |
|
Pérdida de interés en el sexo |
54 |
90 |
44 |
81 |
<0,05 |
Fuente: elaboración propia
Cuando se estratificó por gravedad de los síntomas (Tabla 2; Fig 1), la pérdida de libido fue el síntoma más molesto en el análisis inicial (63.33% de las mujeres puntuaron ‘pérdida de interés en el sexo’ con un ‘2’ - ‘bastante’, o ‘3’ - ‘extremadamente’). Los síntomas cognitivos fueron más molestos que los síntomas de estado de ánimo; 57.5% (rango 10-46.67%) de las mujeres calificaron sus síntomas cognitivos como moderados o severos (una puntuación de ‘2’ o ‘3’), en comparación con el 55% (rango 8.33–38.33%) de las mujeres con síntomas cognitivos. En los síntomas cognitivos, la dificultad para concentrarse fue el más propenso a recibir una puntuación de ‘2’ o ‘3’ (58.33% de las mujeres). Pérdida de interés en el sexo fue el síntoma del estado de ánimo más molesto (asignados una puntuación de ‘2’ o ‘3’ por el 38% de las mujeres).

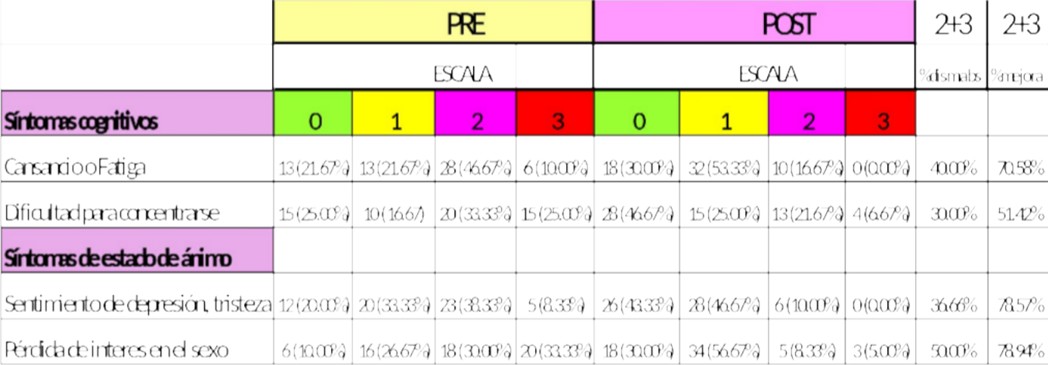
Fuente: elaboración propia
No hubo un aumento en la gravedad de los síntomas, en ninguna mujer, según los MSQ analizados.
Fig. 1 El cambio en la distribución de los puntajes de gravedad de síntomas a lo largo del período de estudio de 6 meses. Los puntajes de ‘3’ (‘extremadamente’) están sombreados de rojo, los puntajes de ‘2’ (‘bastante’) están sombreados de rosa fuerte, los puntajes de ‘1’ (‘un poco’) están sombreados de amarillo, y los puntajes de ‘0’ (‘nada en absoluto’) están sombreados de verde. Se puede observar como desaparece prácticamente el grado de severidad 3 (rojo) para algunos síntomas, lo que indica mejora de los síntomas. Para cada síntoma, solo se incluyen los pacientes que reportaron síntomas en el inicio del tratamiento (puntaje 1, 2 o 3)
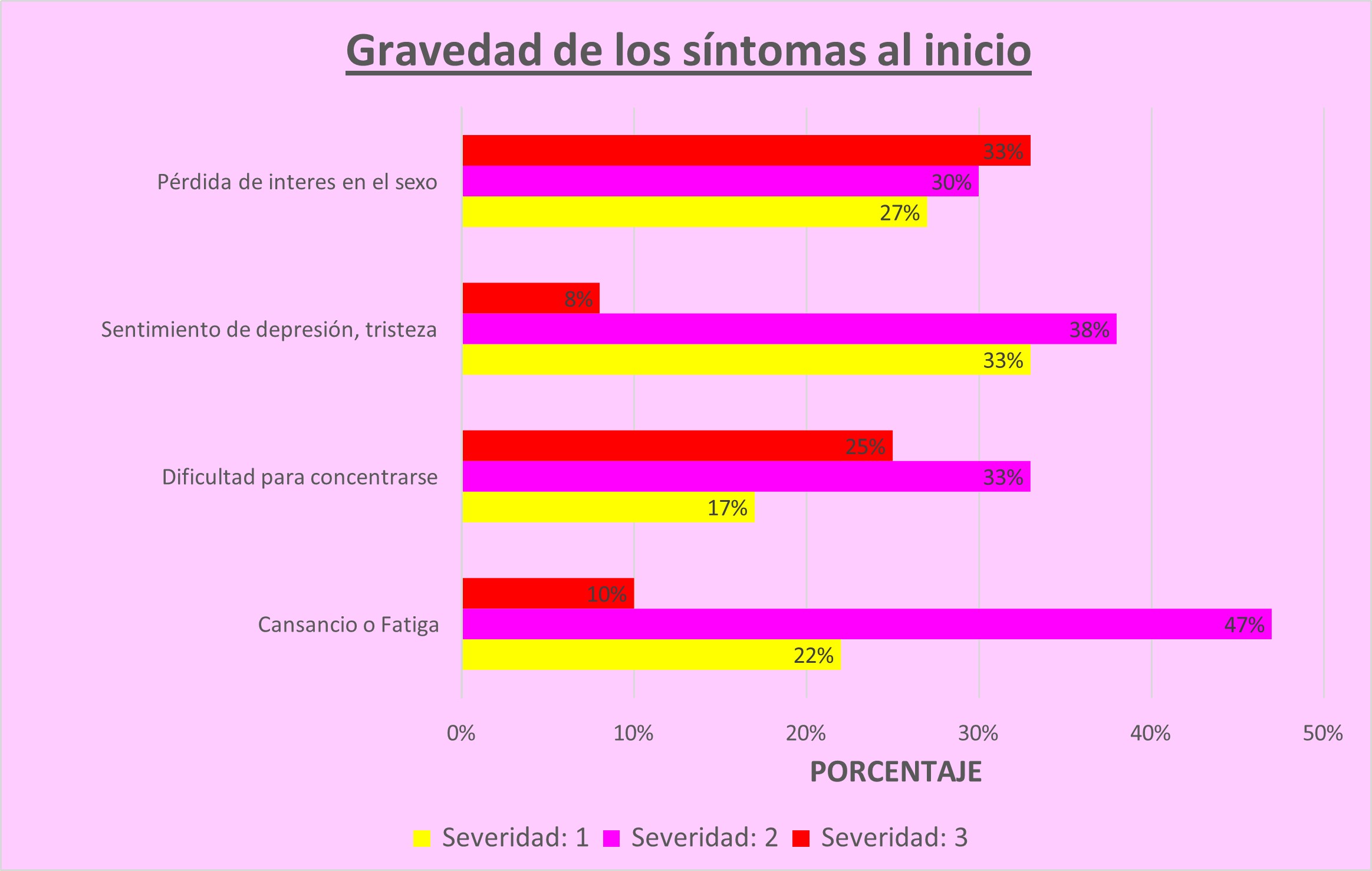
Fuente: Elaboración propia
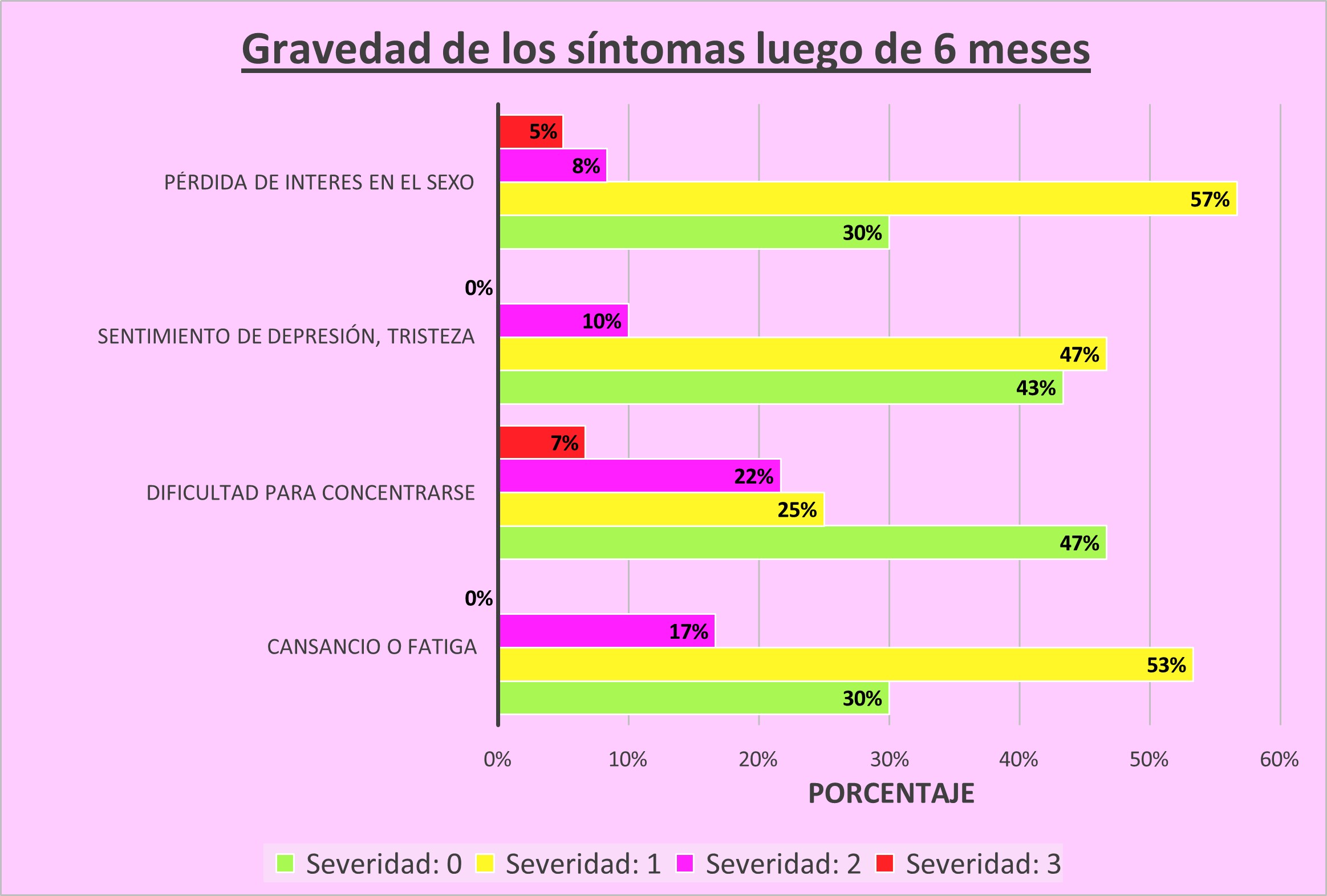
Fuente: elaboración propia
Puntajes de gravedad de síntomas
Los puntajes promedio de síntomas en la línea de base y cuatro meses después de iniciar la terapia de testosterona, y el cambio en los puntajes promedio de síntomas, se presentan en la Tabla 3; Fig. 2.
Tabla 3: Puntaje promedio de síntomas al inicio y a los 6 meses después de iniciar la terapia con testosterona y el cambio en el puntaje promedio de síntomas.
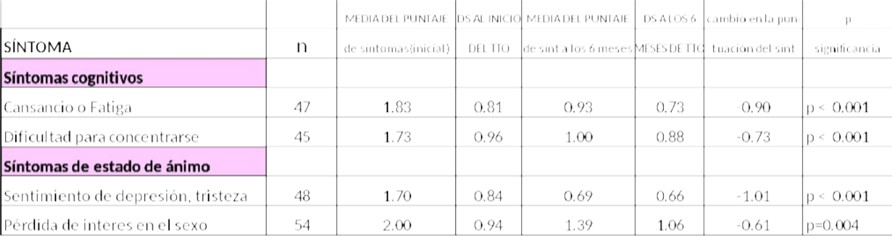
Fuente: elaboración propia
En la línea de base, ‘pérdida de interés en el sexo’ y ‘sentirse cansada o con fatiga lograron los puntajes de síntomas más altos.
Las 4 puntuaciones de síntomas mejoraron significativamente durante el periodo de 6 meses evaluados. Fig 2
Fig 2: El cambio porcentual (mejora) en la puntuación media de síntomas desde el inicio de tratamiento hasta 6 meses después de iniciar la terapia con testosterona.
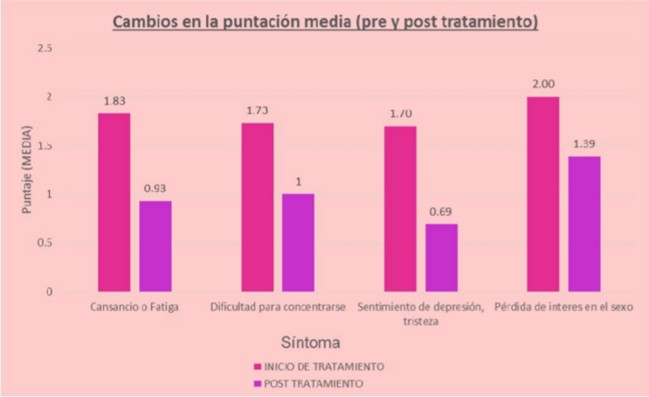
Fuente: elaboración propia
Comentarios (Discusión) Conclusiones
La terapia de testosterona transdérmica idéntica a la del cuerpo durante seis meses se asoció con mejoras significativas en todos los síntomas del estado de ánimo y cognitivos (reducciones en la frecuencia y gravedad de los síntomas) en mujeres perimenopáusicas y posmenopáusicas que asistían al Hospital en un programa llamado mujer activa sito en Garupá (Misiones).
No se ha establecido la seguridad de la terapia con testosterona a largo plazo.
En consecuencia, es probable que el beneficio observado durante el período del estudio resultara del uso de testosterona transdérmica.
Los cuestionarios se completaron en tiempo real, en la línea de base y en el momento de la consulta de revisión, reduciendo el riesgo de sesgo de recuerdo.
La mejora clínica puede, representar un efecto placebo o resultar de factores de confusión no ajustados en nuestro análisis. Por ejemplo, no incluimos datos en el estudio sobre el efecto de la testosterona en otros síntomas menopáusicos como los sofocos nocturnos y el insomnio, que también pueden afectar negativamente el estado de ánimo y la cognición.
La testosterona transdérmica generalmente se tolera bien (Davis et al. 2019; Parish et al. 2021) y, en nuestra experiencia clínica, pocas mujeres interrumpen el tratamiento debido a efectos secundarios. Sin embargo, otros factores como la incomodidad, el olvido y la falta de beneficio percibido (posiblemente debido a una mala absorción transdérmica - discutido más adelante), pueden resultar en una adherencia subóptima y limitar los beneficios potenciales asociados con la terapia de testosterona. En tercer lugar, hay una variación interindividual significativa en la absorción de medicamentos transdérmicos (Farahmand y Maibach 2009; Singh y Morris 2011), y algunas mujeres necesitan dosis más altas para alcanzar niveles fisiológicos. Para el propósito de este estudio, no recopilamos datos sobre los niveles de testosterona sérica antes y durante el tratamiento, y por lo tanto no pudimos confirmar si se alcanzaron niveles fisiológicos en todas las mujeres.
Dado que todas las mujeres recibieron una dosis estándar de testosterona, es poco probable que se alcanzaran niveles terapéuticos en toda la cohorte y se necesita más investigación para evaluar la respuesta clínica tras la optimización de la dosis.
No obstante, durante largo tiempo el uso de la testosterona para el tratamiento de la disfunción sexual femenina fue limitado debido a la falta de preparaciones de uso específico en las mujeres. Las dosis requeridas representan la décima parte de las que se utilizan en el hipogonadismo masculino.
Históricamente, se habían aprobado algunas formulaciones para mujeres. Los implantes (pellets) de testosterona de Organon fueron aprobados para su uso en Australia, pero ya no están disponibles. La metiltestosterona oral, combinada con estrógenos equinos conjugados o estrógenos esterificados, nunca fueron aprobados formalmente para el tratamiento de la disfunción sexual en mujeres posmenopáusicas en los Estados Unidos. Estas formulaciones no fueron evaluadas específicamente para el trastorno de deseo sexual hipoactivo
En Europa se había probado un parche transdérmico para mujeres que liberaba 300 µg de testosterona cada 24 horas (cifra en el límite superior de la producción diaria estimada en una mujer joven), a lo largo de 3 – 4 días (aplicación dos veces por semana).
Una crema transdérmica de testosterona al 1% (AndroFeme, Lawley Pharmaceuticals, Perth, Australia) está disponible para venta bajo receta médica en Australia, aprobada en 2020 por el Registro Australiano de Productos Terapéuticos para el tratamiento del trastorno de deseo sexual hipoactivo en mujeres posmenopáusicas. Esta es la referencia más cercana que tenemos. Está también disponible en UK.
Cuando iniciamos el uso de testosterona en gel, en Argentina, no se disponían marcas comerciales en el mercado aprobados por el ANMAT, por lo tanto, se debió utilizar un preparado magistral, que cumplieron con los estándares de la industria para la pureza, contenido y estabilidad de los ingredientes farmacéuticos activos y las Buenas Prácticas de Fabricación, lo que tiene como base, la testosterona para hombres inspeccionados por ANMAT para asegurar la calidad de fabricación. Cabe señalar que, en la actualidad, se dispone de una sola marca comercial que lo elabora el LABORATORIOS BETA, que se encuentra aprobado por ANMAT.
Por lo tanto, se le adjudica una modesta, pero significativa mejoría en mujeres con menopausia natural y trastorno del deseo sexual hipoactivo, e incluso en mujeres posmenopáusicas que no recibían tratamiento con estrógenos.
Resulta importante señalar que la terapia con testosterona, debe iniciarse después de una completa evaluación biopsicosocial y del manejo adecuado de otras condiciones que pueden contribuir a la disminución del deseo sexual, tales como dispareunia, fatiga secundaria a síntomas vasomotores,anemia, enfermedades de la tiroides, ansiedad, depresión, efectos secundarios de medicamentos y problemas de relación. Si bien, la presencia de estas condiciones no impide en forma absoluta comenzar con el tratamiento con la testosterona, siempre y cuando, las condiciones identificadas estén siendo tratadas y abordadas en forma simultánea. Por lo que se concluye en discusiones anteriores que tanto, la terapia psicológica como la farmacológica se puede combinar, siempre y cuando se considere apropiado.
Agradecimientos:
- Al Hospital Nuestra Señora de Fátima y a su Directora Marta Ruiz, que nos apoyó en todo momento para la realización de éste trabajo en dicho Establecimiento.
Referencias Bibliográficas
- Reuben R, Karkaby L, McNamee C et al (2021) Menopausia y quejas cognitivas: ¿están las hormonas ováricas relacionadas con el declive cognitivo subjetivo? Quejas cognitivas: ¿están las hormonas ováricas vinculadas con el declive cognitivo subjetivo? Climacteric 24:321–332. https://doi.org/10.1080/13697137.2021.1892627.
- Leonhardt M (2019) Estado de ánimo bajo y síntomas depresivos durante la perimenopausia – ¿deberían los médicos generales prescribir terapia de reemplazo hormonal o antidepresivos como tratamiento de primera línea? Post Reprod Heal 25:124–130. https://doi.org/10.1177/2053369119847867.
- Davis SR (2023) Testosterona para mujeres: certezas e ties. Climacteric 26:21–24. https://doi.org/10.1080/13697137.2022.2146492.
- Davis SR, Jane F, Robinson PJ et al (2014) Testosterona transdérmica mejora el aprendizaje verbal y la memoria en mujeres posmenopáusicas que no están en terapia de estrógenos. Clin Endocrinol 81:621–628. https://doi.org/10.1111/cen.12459.
- Islam RM, Bell RJ, Green S, et Seguridad y eficacia de testosterona para mujeres: una revisión sistemática y metaanálisis de datos de ensayos controlados aleatorios. Lancet Diabetes Endocrinol 2019;7:754–766.
- Davis SR, Baber R, Panay N, et Declaración de consenso global sobre el uso de la terapia de testosterona para mujeres. J Sex Med 2019;16:1331–1337.
- Parish SJ, Simon JA, Davis SR et al (2021) Sociedad Internacional para el Estudio de la Salud Sexual de las Mujeres Guía de Práctica Clínica para el uso de testosterona sistémica para el Trastorno de Deseo Sexual Hipoactivo en Mujeres. J Sex Med 18:849–867. https://doi.org/10.1016/j.jsxm.2020.10.009.
- Islam RM, Bell RJ, Green S et al (2019) Seguridad y eficacia de la testosterona para mujeres: una revisión sistemática y un metaanálisis de datos de ensayos controlados aleatorizados. Lancet Diabetes Endocrinol 7:754–766. https://doi.org/10.1016/s2213- 8587(19)30189-5.
- NICE (2019) Menopausia: diagnóstico y En: Menopausia: diagnóstico y manejo. www.nice.org.uk/guidance/ng23. Accedido el 20 de agosto de 2024.
- Davis SR, Baber R, Panay N et al (2019) Declaración de consenso global sobre la terapia de testosterona para J Clin Endocrinol Metab 104:4660–4666. https://doi.org/10.1210/jc.2019-01603.
Agradecimientos
- Al Hospital Materno neonatal y a la Farmacéutica Nancy Alarcón, quien nos facilitó el Laboratorio de preparados magistrales.
- A la Técnica en Esterilización Isaura Altamirano, quien colaboró activamente en el fraccionamiento envasado de los productos.
ANEXO: 1

ANEXO 2: EQUIPO MULTIDISCIPLINARIO
- DR BÁEZ GABRIEL FRANCISCO MÉDICO ESPECIALISTA EN TOCOGINECOLOGIA CALIFICACIÓN AGREGADA EN CLIMATERIO
- Farmacéutica Juliana Elisa Britez, Especialista en Esterilización. Especialista en Farmacia Clínica.
- Dra Fochesatto Noelia Alejandra, Especialista en ginecología y obstetricia Especialista en ecografía.
- Kühle Ana Alicia Licenciada en enfermería, Diplomatura en políticas públicas y gestión.
- Wimer Pamela Judith, Psicologa, Sexóloga. Especialista en infertilidad, Especialista en salud materno infantil.
- Marianela Licenciada en Nutrición. Antropometrista ISAK nivel II

ANEXO 3
MSQ: CUESTIONARIO DE SÍNTOMAS DE MENOPAUSIA
ESCALA CLIMATÉRICA DE GREENE (Greene JG. Constructing a standard climateric scale) MODIFICADA
Identificador: Fecha:
Marque con una tilde el cuadro que corresponda a la intensidad con la que actualmente presenta los siguientes síntomas:
|
SÍNTOMAS |
NADA |
UN POCO |
BASTANTE |
INTENSAMENTE |
|
(0) |
(1) |
(2) |
(3) |
|
|
1- Cansancio / fatiga |
⃝ |
⃝ |
⃝ |
⃝ |
|
2- Dolores musculares |
⃝ |
⃝ |
⃝ |
⃝ |
|
3- Dificultad para concentrarse |
⃝ |
⃝ |
⃝ |
⃝ |
|
4- Disminución del deseo sexual |
⃝ |
⃝ |
⃝ |
⃝ |
|
5- Sudores nocturnos |
⃝ |
⃝ |
⃝ |
⃝ |
|
6- Sentimientos de infelicidad o depresión |
⃝ |
⃝ |
⃝ |
⃝ |
|
7- Dificultad para dormir |
⃝ |
⃝ |
⃝ |
⃝ |
|
8- Irritabilidad |
⃝ |
⃝ |
⃝ |
⃝ |
|
9- Mal humor |
⃝ |
⃝ |
⃝ |
⃝ |
|
10- Calores / sofocos |
⃝ |
⃝ |
⃝ |
⃝ |
ANEXO 4

-
Médico/a Tocoginecólogo/a
- Lic en Enfermería
- Lic en Nutrición
- Lic. en Psicología
