Guía de Manejo de las Alteraciones del Piso Pélvico 2023
Autores:
Dra. Adelaida Garcia, Dr. Rene German Laurito, Dra. Lucila Pavan, Dr. Gonzalo Martinez, Dr. Javier Vila, Dra. Marta Ledesma, Dra. Lorena Roca, Dr. Mariano Rosini, Dr. Santiago Orrico,
Introducción
Las alteraciones del piso pélvico abarcan una serie de modificaciones anatómicas y funcionales que afectan principalmente a la mujer. Las pacientes consultan por incontinencia de orina (IO), incontinencia fecal (IF) y prolapso de órganos pélvicos como único síntoma o combinados. Se trata de un motivo de consulta frecuente, que afecta la calidad de vida de las mujeres que lo padecen. Los datos epidemiológicos existentes son muy variables, se trata de una patología subreportada y subdiagnosticada que se considera cada vez mas prevalente, debido al aumento de la expectativa de vida de la mujer.
El piso pélvico está formado por un conjunto de estructuras musculares, de fascias y ligamentos que forman lo que se conoce como diafragma urogenital , y tienen como misión básica el sostén de los órganos pélvicos (vejiga, uretra, útero, vagina, recto y ano). Dichos componentes músculo- aponeuróticos no sólo deben mantener la correcta posición de los órganos, sino que además deben permitir y facilitar sus funciones como: la micción, el coito, la defecación, y el parto, asegurando al mismo tiempo la continencia urinaria y fecal en reposo y durante las actividades de la vida diaria.
La debilidad o la lesión de los elementos que forman el piso pélvico predispone a la mujer a una sintomatología en muchas ocasiones múltiple, que corresponde a la combinación de distintos problemas, como la IO, la IF, la disfunción del vaciado vesical, la constipación tipo outlet (defecación obstructiva), el prolapso de órganos pélvicos y la disfunción sexual.
- Lacima, , & Espuña, M. (2008). Patología del suelo pélvico. Gastroenterología y Hepatología, 31(9), 587–595. doi:10.1157/13128299
- WEI, T., & DE LANCEY, J. O. L. (2004). Functional Anatomy of the Pelvic Floor and Lower Urinary Tract. Clinical Obstetrics and Gynecology, 47(1), 3–17.
INCONTINENCIA DE ORINA DE ESFUERZO
Definición
La definición más aceptada por todas las sociedades es aquella realizada por la IUGA(International Urogynecological Association) y la ICS (International Continence Society) en el reporte conjunto de terminología para las disfunciones del piso pélvico que define a la incontinencia de orina de esfuerzo (IOE) como la queja de pérdida involuntaria de orina que sucede ante el esfuerzo físico y/ o el incremento de la presión intraabdominal durante el estornudo, la tos, o la risa.1
La fisiopatología de la IOE responde a dos mecanismos, los cuales se superponen en muchas ocasiones: la hipermovilidad uretral y la deficiencia esfinteriana intrínseca (defecto en la coaptación uretral).
En 1994 Delancey propone la “teoría de la hamaca” para explicar la funcionalidad anatómica del suelo pélvico, describiendo que el cuello vesical y la uretra se sostienen por una hamaca formada por los músculos de la porción anterior de la vagina insertos sobre el arco tendinoso de la fascia pélvica, los cuales, ante aumentos de la presión intraabdominal generan una compresión de la uretra. Esta compresión, sumada a la presión esfinteriana intrínseca, mantienen a la uretra en su posición correcta, cerrada, evitando la pérdida involuntaria de orina.4
La lesión o debilitamiento de los músculos del suelo de la pelvis, y/o la desinserción del arco tendinoso de la fascia pélvica producen una pérdida del sostén de la uretra, aumentando su motilidad ante los aumentos de la presión intra abdominal.5
Los factores de riesgo más aceptados son:
- edad: 3% de las mujeres mayores de 35 años; 7% entre 55 y 64 años, y 38% de las mujeres mayores de 70 años presentan
- obesidad: incrementa tres veces el riesgo de IOE (esto se debe al aumento persistente de la presión intrabdominal)
- paridad /vía de nacimiento: la multiparidad, los partos instrumentales o
- otras comorbilidades: diabetes (por la denervación), enfermedad pulmonar crónica (la tos crónica aumenta la presión intraabdominal), menopausia (por la disminución del trofismo), tabaquismo (alteración de la vascularización), radioterapia pelviana, histerectomía (cambio del eje vaginal), ejercicio de alto impacto (por el aumento persistente de la presión intraabdominal).
Epidemiología
Las estimaciones de la prevalencia y la incidencia varían ampliamente, debido a que no hay definiciones epidemiológicas estandarizadas o consistentes para IO o IOE 6.
Aproximadamente el 50 % de las mujeres con IO informan que la IOE es el principal o único síntoma de incontinencia. En la Encuesta de Salud Nacional y Examen de Nutrición (NHANES de EEUU) confirman estas aproximaciones, según datos de la encuesta de 2001 a 2004, el 49,6% de las mujeres informaron cualquier IO, con 49.8% reportando IOE pura, 34.4% IOM y 15,9 % IOU 2,3. Wallner et al evaluó la prevalencia de IO en mujeres sin diagnóstico de IO y determinó que la prevalencia ajustada por edad de IOE no diagnosticada era del 18,7%, por este motivo se debe realizar un interrogatorio dirigido con el fin de buscar la patología.
Diagnostico
El valor de una historia clínica completa y un examen físico sigue siendo indiscutible. Evaluar frecuencia miccional diurna y nocturna, tipo de incontinencia, antecedentes de trastornos del vaciado, síntomas sexuales, gastrointentinales y neurológicos. La utilización del diario miccional para objetivar lo recabado en la historia clínica es de gran utilidad, particularmente cuando hay sintomas asociado a la IOE.
Los estudios observacionales han demostrado que los diarios miccionales tienen reproducibilidad satisfactoria, factibilidad, confiabilidad y validez. La duración óptima del diario se sugiere entre 3 y 7 días. Sin embargo en la práctica diaria, puede no ser aceptado por parte de la paciente la realizacion del diario de manera prolongada, brindando informacion util, la realizacion de un diario miccional de 48 hs.
El examen clínico debe incluir un examen abdominal y genitourinario, tono y función del músculo elevador del ano, valorar IO con la valsalva en pacientes con vejiga llena, un volumen vesical de al menos 200 ml se ha asociado a una buena sensibilidad, hipermovilidad uretral (mediante el Q-tip test), y trofismo vaginal.
La valoración inicial debe incluir un análisis de orina para descartar infecciones del tracto urinario. Estas son una causa común de trastornos miccionales. Y la valoración del residuo posmiccional, si bien no existe un consenso sobre cual es el valor que se considera como patológico, un RPM > a 150 ml, nos debería alertar de la necesidad de valorar le función del detrusor. Y por lo tanto solicitar como parte de la evaluación, un estudio urodinamico (EUD)
La utilidad del EUD en el diagnóstico de la IOE pura ha sido ampliamente discutido. En general, el EUD preoperatorio no modifico el resultado posquirugico en cuanto a tasa de curación entre pacientes con IOE pura, tampoco modifico la decisión terapéutica.
Tratamiento
Manejo conservador
Descenso de peso. El sobrepeso y la obesidad tienen una asociación directamente proporcional con la IOE. Basado en diferentes revisiones sistemáticas y ensayos clínicos randomizados, podemos decir que el descenso de peso no quirúrgico y la cirugía bariátrica mejoran la sintomatología de la IOE en pacientes obesas. Debemos alentar a las pacientes a bajar de peso sean o no candidatas a tratamiento quirúrgico, ya que se ha demostrado el beneficio a largo plazo. (Grado de recomendación A)
Terapias físicas y conductuales:
Reeducación vesical y ejercitación de los músculos del suelo de la pelvis (EMPP).
La reeducación vesical es una estrategía terapéutica que puede ofrecerse a todos los pacientes sin presentar efectos adversos y consiste en instruir al individuo respecto al vaciado de su vejiga y a la ingesta de líquidos, disminuyendo consumo de café y otras bebidas estimulantes. Se indica realizar micciones programadas, y hacer un registro discriminando aquellas micciones que fueron programadas con deseo o sin él. La reeducación vesical es menos efectiva que la EMPP, y que la combinación de esta con biofeedback muestra mejoría de los síntomas.9
La EMPP es un programa de entrenamiento supervisado, en el cual se le enseña a la paciente mediante tacto genital, a realizar la contracción de los músculos del piso de la pelvis. El biofeedback es un programa de entrenamiento de los músculos del piso de la pelvis, asociado a un dispositivo auditivo o visual, a través del cual la paciente puede valorar la contracción muscular que realiza 9.
El objetivo de la rehabilitación perineal es mejorar la fuerza de contracción de los músculos del periné, lo que permitirá una mayor estabilidad de la uretra y una mayor presión de cierre.
Una revisión de 21 ensayos clínicos realizada por el Cochrane determinó que a mayor intensidad y frecuencia de la ejercitación, mayor eficacia (nivel de evidencia 1). Sin embargo la adherencia a esta terapia es muy baja y las pacientes no suelen sostenerlas en el tiempo.10
Las recomendaciones son:
Ofrecer EMPP supervisado e intenso durante 3 meses a todas las pacientes con síntomas de IOE o IOM (grado A)
Ofrecer EMPP a mujeres adultas mayores (grado B)
Considerar uso de biofeedback en el tratamiento de la IOE (grado A)
Manejo quirúrgico
De optarse por éste, la decisión debe ser tomada de forma conjunta con la paciente, quién debe haber sido previamente asesorada respecto a los beneficios, posibles efectos secundarios, y complicaciones de la cirugía.
La cirugía debe ser realizada por un profesional entrenado en la técnica, que mantenga una determinada casuística, y dicho entrenamiento tiene que haber sido brindado por alguien especialista. Debe ser capaz de brindar otras opciones terapéuticas y de resolver las complicaciones quirúrgicas.
Los procedimientos quirúrgicos hasta ahora descritos para el tratamiento quirúrgico de la IOE se clasifican en abdominales (por vía laparotómica o laparoscópica) o vaginales. También se clasifican según el origen del material que utilicen para la suspensión uretral: tejidos autólogos o mallas sintéticas.
- Sling medio uretral libre de tensión: por via retropúbica (RP); por via transobturatriz (TOT)
- Operación de Burch: colposuspensión abdominal vía laparotómica o laparoscópica.
Los parámetros para valorar resultados son: grado de continencia y episodios de incontinencia; complicaciones asociadas al procedimiento; calidad de vida referida por la paciente en cuanto a sintomatología urinaria, defecatoria y sexual.
Un apartado para mencionar la reparación vaginal anterior con puntos de Kelly. Esta técnica quirúrgica fue descripta en 1913 y luego modificada como técnica de Kelly Kennedy en 1937, asociada a la colporrafia anterior, como tratamiento de la IOE. Actualmente es una técnica desaconsejada para el tratamiento de la IOE. La principal causa es su baja eficacia a mediano plazo. En un ECC que comparo la plicatura de kelly vs sling mediouretral al año de seguimiento, fue de 87% para el sling mediouretral, vs 66% para la plicatura de Kelly.
El gold standard para el manejo quirúrgico de la IOE fue durante mucho tiempo la colposuspensión abdominal de Burch, procedimiento en el cual se realizaba una suspensión de la uretra anterior hacia ambos ligamentos pectineos. Esta técnica quirúrgica fue reemplazada por procedimientos minimamente invasivos por vía vaginal. En 1990 Petros y Ulmsten desarrollaron el primer sling de uretra media libre de tension por via retropubica. Esta operación introdujo dos conceptos nuevos, la colocacion del sling en la uretra media, hasta ese momento se colocaban en el cuello de la vejiga y la colocación libre de tensión. Debido a la probabilidad de lesionar la vejiga durante el pasaje a ciegas de la aguja por el espacio retropubico, es que durante el procedimiento se debe realizar una cistoscopia de control. En la etapa inicial, de consolidación de la técnica, se reportaron algunas lesiones raras, pero graves, por lo cual en 2001 Delorme presentó una vía alternativa para la colocación del sling medio uretral por vía transobturatriz, esta vía alcanzó gran popularidad.
Revisiones que compararon la colposuspensión de Burch con los sling medio uretrales no evidenciaron diferencias en la tasa de respuesta, pero demostraron diferentes perfiles de complicaciones, siendo más frecuentes las disfunciones del vaciado, mayor tiempo quirúrgico, mayor morbilidad en la cirugía a cielo abierto, uretra fija y enterocele luego de la colposuspensión abdominal y más frecuente el riesgo de perforación vaginal o vesical durante el sling retropubico.
El metaanálisis realizado durante el desarrollo de las guías de la EAU para el manejo de la incontinencia urinaria, citada previamente, incluyó alrededor de 5800 pacientes y comparó el sling retropubico versus el transobturatriz observando una similar tasa de cura a 12 meses, siendo más frecuente el desarrollo de alteraciones del vaciado, lesión vesical o ureteral luego de un retropubico, pero más frecuente el dolor inguinal crónico postoperatorio y necesidad de repetir la cirugia antiincontinencia luego de un transobturatriz.
Resumiendo la evidencia respecto al manejo quirúrgico de la IOE queda establecido que:
- la tasa de curación a 12 meses es similar para procedimientos abdominales y sling medio uretrales (nivel de evidencia 1a);
- la aparición de incontinencia de urgencia de novo u otras disfunciones del vaciado son más frecuentes con la colposuspensión abdominal, el sling RP y el TOT en orden decreciente ( evidencia 1a)
- El riesgo de lesión vesical y uretral es más frecuente con el RP que con el TOT (nivel de evidencia 1 a)
- La incidencia de dolor pelviano crónico luego de 12 meses postoperatorio es mayor con el TOT que con el RP (nivel de evidencia 1a)
Una de las más recientes publicaciones consistente en una revisión sistemática y análisis económico sobre las diferentes técnicas de tratamiento quirúrgico de la incontinencia urinaria publicada en 2019 concluyó que el uso de sling medio uretrales ya sea retropúbico o transobturatriz son más efectivos a corto y mediano plazo en comparación con otras técnicas y costo efectivos a largo plazo.12
Sustancias de abultamiento
La aplicación de sustancias de abultamiento tiene como objetivo generar un relleno en la mucosa suburetral para permitir mejor coaptación del esfínter y por ende resolver la incontinencia.
Es un procedimiento sencillo que consiste en la inyección transuretral o periuretral, bajo visión directa con cistoscopio.
Puede considerarse como opción terapéutica en pacientes que presenten una incontinencia de esfuerzo sin hipermovilidad uretral, en aquellas pacientes que aún no han cumplido la paridad, o en quienes tienen contraindicación para una cirugía mayor por obesidad, anticoagulación, edad avanzada u otras condiciones que impliquen un alto riesgo anestésico. También puede ser considerado como una opción de rescate luego de un sling medio uretral con resultados insatisfactorios. Los posibles efectos adversos incluyen incontinencia de orina de urgencia de novo, reacción inmune, hematuria, retención aguda de orina, granuloma.13
Las sustancias de abultamiento no deben usarse como primera línea terapéutica en aquellas pacientes que no presenten contraindicación para una intervención quirúrgica. 14
La eficacia terapéutica es limitada, es una tratamiento de alto costo y requiere inyecciones periódicas.
Bibliografía
- Bernard T. Haylen & Dirk de Ridder et al. An International Urogynecological Association (IUGA)/ International Continence Society (ICS) joint report on the terminology for female pelvic floor Int Urogynecol J (2010) 21:5–26 DOI 10.1007/s00192-009-0976-9 )
- Pizzol D., Demurtas J., Celotto S., Maggi S., Smith L., Angiolelli G., Trott M., Yang L., Veronese N. Urinary incontinence and quality of life: A systematic review and meta-analysis. Aging Clin. Exp. 2021;33:25–35. doi: 10.1007/s40520-020-01712-y)
- Linda Incontinence, 7th edition. 2023.
- John L Delancey, James A Ashton-miller, Pathophysiology of adult urinary incontinence, Gastroenterology, Volume 126, Supplement 1, 2004, Pages S23-S32, ISSN 0016-5085, https:// doi.org/10.1053/j.gastro.2003.10.080.)
- Nambiar A.K., Bosch R., Cruz F., Lemack G.E., Thiruchelvam N., Tubaro A., Bedretdinova D.A., Ambühl , Farag F., Lombardo R., et al. EAU Guidelines on assessment and nonsurgical management of urinary incontinence. Eur. Urol. 2018;73:596–609. doi: 10.1016/ j.eururo.2017.12.031)
- Stuart Reynolds & Roger R. Dmochowski & David F. Penson. Epidemiology of Stress Urinary Incontinence in Women. Curr Urol Rep (2011) 12:370–376
- Godfrey A. Walker & Prasanna Gunasekera. Pelvic organ prolapse and incontinence in developing countries: review of prevalence and risk factors. Int Urogynecol J (2011) 22:127–135
- Nambiar, K. et al. European Association of Urology Guidelines on the Diagnosis and Management of Female Non-neurogenic Lower Urinary Tract Symptoms. Part 1: Diagnostics, Overactive Bladder, Stress Urinary Incontinence, and Mixed Urinary Incontinence. European Urology, Vol. 82 Nr. 1 Páginas: 49 - 59. 2022
- Oliveira M, Ferreira M, Azevedo MJ, Firmino-Machado J, Santos PC. Pelvic floor muscle training protocol for stress urinary incontinence in women: A systematic review. Rev Assoc Med Bras (1992). 2017 Jul;63(7):642-650. doi: 1590/1806-9282.63.07.642.)
- Hay-Smith EJ, Herderschee R, Dumoulin C, Herbison GP. Comparisons of approaches to pelvic floor muscle training for urinary incontinence in women. Cochrane Database Syst Rev. 2011 Dec 7; (12):CD009508. doi: 10.1002/14651858.CD009508. PMID: 22161451)
- Freites J, Stewart F, Omar MI, Mashayekhi A, Agur WI. Laparoscopic colposuspension for urinary incontinence in women. Cochrane Database Syst Rev. 2019 Dec 10;12(12):CD002239. doi: 1002/14651858.CD002239.pub4. PMID: 31821550; PMCID: PMC6903454.)
- Brazzelli M, Javanbakht M, Imamura M, Hudson J, Moloney E, Becker F, Wallace S, Omar MI, Shimonovich M, MacLennan G, Ternent L, Vale L, Montgomery I, Mackie P, Saraswat L, Monga A, Craig D. Surgical treatments for women with stress urinary incontinence: the ESTER systematic review and economic evaluation. Health Technol Assess. 2019 Mar;23(14):1-306. doi: 10.3310/ )
- Mamut A, Carlson KV. Periurethral bulking agents for female stress urinary incontinence in Can Urol Assoc J. 2017 Jun;11(6Suppl2):S152-S154. doi: 10.5489/cuaj.4612.)
- Nambiar A.K., Bosch R., Cruz F., Lemack G.E., Thiruchelvam N., Tubaro A., Bedretdinova D.A., Ambühl , Farag F., Lombardo R., et al. EAU Guidelines on assessment and nonsurgical management of urinary incontinence. Eur. Urol. 2018;73:596–609. doi: 10.1016/ j.eururo.2017.12.031)
INCONTINENCIA DE ORINA DE URGENCIA
Definición:
La vejiga hiperactiva (VHA) es definida por la ICS1 como la presencia de “urgencia urinaria, usualmente acompañada por frecuencia y nocturia, con o sin incontinencia de orina, en ausencia de infección urinaria u otra patología evidente”.
Es decir que es un síndrome que se caracteriza por estos tres síntomas, urgencia 2 llamada a la necesidad imperiosa de orinar que no se puede posponer; frecuencia 3, que es la queja del aumento del número de micciones durante el día percibido por la paciente (esto va a depender del líquido ingerido, pero un número de hasta 7 micciones diarias sería considerado normal 4 y la nocturia 5, que es la queja de la interrupción del sueño uno o más veces debido a la necesidad de orinar.
Como se menciona en su definición la vejiga hiperactiva puede ser “seca” si la paciente no presenta episodios de incontinencia urinaria, o “húmeda” cuando sí los presenta. A esta última conocida cómo incontinencia de orina de urgencia (IOU) que es la pérdida involuntaria de orina precedida por un deseo imperioso de orinar 6.
Otro punto a destacar en la definición de VHA es que para diagnosticar este síndrome debemos descartar, como ya veremos más adelante, otras patologías del tracto urinario inferior que podrían provocarla (infección urinaria, diverticulo de uretra, prolapso de órganos pelvianos, etc)
Epidemiologia
En estudios basados en la población, las tasas de prevalencia de VHA oscilan 9% a 43% en mujeres. La IOU es consistentemente más común en las mujeres que en los hombres. La prevalencia y gravedad de los síntomas de la VHA tienden a aumentar con la edad 7.
Aunque los síntomas de la VHA son tan comunes en la población, muchas pacientes no hablan de este problema que las afecta. Solo el 60% de las personas con síntomas de incontinencia buscan ayuda y solo el 27% reciben tratamiento 5. Las razones de la demora en la búsqueda de asesoramiento incluyen la aceptación de síntomas como una parte normal del envejecimiento, particularmente en personas mayores, y el temor inherente de que la cirugía sea el único tratamiento. Como resultado, sin duda, hay un gran población oculta de pacientes con vejiga hiperactiva no tratada 8.
Diagnostico
Los 3 pilares fundamentales para realizar un correcto diagnóstico del síndrome de la VHA deben ser:
- Interrogatorio Dirigido: Es fundamental preguntar sobre los 3 síntomas que caracterizan al síndrome (urgencia, frecuencia y nocturia) así también como otros problemas de almacenamiento (p. ej., incontinencia de esfuerzo) o vaciamiento de la vejiga (por ejemplo, vacilación, esfuerzo para orinar, historia previa de retención urinaria, fuerza del chorro, intermitencia del chorro)
- ¿Cuándo tiene deseos de orinar, debe buscar un baño en ese momento o puede aguantar?
- ¿Va muchas veces al baño a orinar? (No olvidar que es la percepción de la paciente que va más veces al baño de lo normal)
- ¿Se levanta por la noche a orinar? ¿Cuántas veces?
- Pierde orina cuando tose, estornuda o hace algún esfuerzo
- ¿Cuándo orina, el chorro es normal? ¿Le cuesta comenzar a orinar? ¿Tiene la sensación de no vaciar completamente la vejiga?
Debemos interrogar también:
- Hábitos en la ingesta de líquidos (polidipsia, necesidad de beber con frecuencia y abundantemente) 9
- Comorbilidades (edema de miembros inferiores, insuficiencia cardiaca, afecciones renales, Hipertensión arterial, diabetes).
- Medicación habitual que pueden alterar el ritmo miccional (diuréticos, etc).
- Hábitos de higiene (la higiene excesiva altera la flora habitual produciendo en muchos casos irritación vesical).
- Movilidad: la movilidad reducida, la utilización de bastón, andador, silla de ruedas dificulta muchas veces la llegada al baño a
Examen físico:
Examen genitourinario: se realiza en posición ginecológica. Se debe evaluar: Prolapso de órganos pelvianos, contractura de los músculos del elevador del ano, examinar la uretra en búsqueda de tumoraciones (diverticulo, carúncula uretral). En mujeres menopáusicas, la atrofia urogenital debe evaluarse como posible contribuyente de los síntomas de VHA.
Examen abdominal: evaluar cicatrices, masas, hernias y áreas de sensibilidad, así como la distensión suprapúbica que puede indicar retención urinaria.
También es importante evaluar las extremidades inferiores por el edema, dado que puede ser un factor determinante durante los períodos de cambios posturales (al acostarse durante la noche se produce reabsorción de los edemas, con formación de orina y asi presentando síntomas de nocturia)
Urocultivo: La realización de un análisis de orina descarta la infección urinaria, la cual puede ser causa de los síntomas manifestados por la paciente.
Diario urinario: mencionado previamente
Medición de residuo post miccional: No debería pedirse de rutina en casos donde no hay sospecha de obstrucción urinaria o sospecha de residuo elevado 10. En el caso de utilizar antimuscarínicos o agonistas b, los cuales pueden causar retención urinaria, y en pacientes con trastornos del vaciado vesical en donde podrían empeorar sus síntomas, solicitar ecografía con medición de residuo.
Estudio URODINÁMICO: no debe ser solicitado en pacientes con vejiga hiperactiva de inicial abordaje. El mismo es un estudio invasivo, con baja sensibilidad para la detección de hiperactividad del detrusor (esto quiere decir que un estudio normal no descarta el diagnóstico de VHA y la paciente debería ser tratada por la sintomatología que manifiesta). Se debe dejar reservado para casos de vejiga hiperactiva refractaria al tratamiento o en algunos casos especiales donde el interrogatorio y la sospecha diagnóstica está en duda 10.
Tratamiento
El tratamiento de la VHA es un tratamiento escalonado, yendo de conductas menos invasivas y simples, que puedan ser mantenidas a lo largo del tiempo hasta la inclusión de medicación o tratamientos más invasivos.
La idea es acompañar en este proceso a la paciente, sin retrasar diagnósticos ni tratamientos, estimulando en la paciente la adherencia, mantenimiento o avance en el tratamiento. Para optimizar la eficacia, es fundamental que los pacientes tengan claro las expectativas con respecto a los posibles efectos del tratamiento y eventos adversos 7.
En cada escalón, la paciente debe comprometerse y participar activamente para poder modificar estilos de vida. Las terapias conductuales requieren una inversión de tiempo y esfuerzo por parte del paciente para lograr los máximos beneficios y puede requerir contacto regular con el médico para mantener adherencia al régimen y la consecuente eficacia 12.
Cambios conductuales:
Aunque la mayoría de las pacientes no experimentan un alivio completo de los síntomas con los cambios conductuales la literatura indica que la mayoría experimentan reducciones significativas en síntomas y mejoras en la calidad de vida. ((7)). Duración ideal 4-8 semanas y reevaluar.
Se basa en medidas higiénico dietéticas como:
Restricción de líquidos ingeridos en todo el día de hasta 1.5lts 11
Suspender ingesta de líquidos 3-4 hs previo a acostarse
Higiene de la zona genital 1 vez por día al bañarse, evitando duchas vaginales, jabones íntimos o toallitas húmedas.
Micciones programadas: reentrenamiento vesical aumentando la frecuencia de micciones. Kinesiología del piso pélvico: biofeedback de piso pelviano, electroestimulación de nervio tibial posterior, fortalecimiento de músculos del piso de la pelvis, relajación, medidas evitativas de urgencia, etc.12
Tratamiento farmacologico:
Los estrógenos locales constituyen junto a la terapia conductual la primera linea de abordaje.
El segundo eslabón consiste en sumar a los cambios conductuales la medicación. Se reserva la medicación como segunda línea dado que a pesar de que pueden producir mejoría de los síntomas, muchas veces no están exentos de efectos adversos. Duración ideal 4-8 semanas y reevaluar
Anticolinergicos: su efecto es el bloqueo de receptores muscarínicos a nivel vesical para disminuir las contracciones de la misma
En Argentina hay varios agentes antimuscarínicos disponibles pero actualmente solo en preparaciones por vía oral. Tienen una tasa de eficacia para el tratamiento de la VHA del 65-70 % en la reducción de los síntomas principales 13. Los efectos secundarios, como sequedad de boca y estreñimiento, pueden resultar molestos para algunos pacientes a pesar de su eficacia. Además, dado que estos agentes tienen la capacidad de unirse y bloquear los receptores muscarínicos en todo el cuerpo, incluidos los del cerebro, existe preocupación con respecto a la carga anticolinérgica en pacientes de edad avanzada que contribuye a eventos adversos como caídas, estreñimiento, deterioro cognitivo y desarrollo de delirio 13. Debido a la eficacia similar observada para todos los antimuscarínicos, la elección del medicamento para un paciente en particular depende de la historia del paciente de uso de antimuscarínicos, información sobre efectos adversos experimentados en el pasado, el uso de otros medicamentos 7.
|
DROGA |
DOSIS |
UROSELECTIVO |
EFECTO ADVERSO |
|
OXIBUTININA |
5–15 mg/dia |
NO |
BOCA SECA 68% CONSTIPACIÓN 10% DETERIORO CONGNITIVO |
|
SOLIFENACINA |
5–10 mg/día |
SI |
BOCA SECA 26% CONSTIPACIÓN 12% VISIÓN BORROSA 5% |
|
DARIFENACINA |
7.5–15 mg/día |
SI |
BOCA SECA 35% CONSTIPACIÓN 21% |
|
TOLTERODINA |
2 mg dos veces por dia |
NO |
BOCA SECA 23% CONSTIPACIÓN 6% OJO SECO 4% |
|
TROSPIUM |
20 mg dos veces por día |
NO |
BOCA SECA 22,8% CONSTIPACIÓN 9,5% DOLOR ABDOMINAL 3,1% |
Agonista beta: el mirabegron actúa para facilitar la relajación del detrusor. Los efectos secundarios como la boca seca, son estadísticamente menores en comparación con la terapia antimuscarínica. Además, aunque existen preocupaciones con respecto a los aumentos de la presión arterial, estos siguen siendo pequeños y el mirabegrón es eficaz y seguro, sin diferencias en la hipertensión emergente del tratamiento en comparación con el placebo. La Agencia Reguladora de Medicamentos y Productos para el Cuidado de la Salud recomienda el uso de mirabegrón con precaución en aquellos pacientes con hipertensión en estadio 2 (presión arterial sistólica ≥ 160 mmHg y/o diastólica ≥ 100 mmHg). Está contraindicado en pacientes con hipertensión severa no controlada (presión arterial sistólica ⩾180 mmHg y/o diastólica 100 mmHg)
Se puede considerar la terapia combinada (antimuscarínicos y agonistas beta3) en pacientes refractarios a la monoterapia. La administración conjunta parece mejorar la eficacia con un aumento mínimo en el perfil de efectos secundarios. Se informa que la terapia combinada con solifenacina y mirabegron (en dosis de 5 mg y 25 mg o 5 mg y 50 mg, respectivamente) tiene una disminución estadísticamente significativa en el número de episodios de incontinencia y micción en comparación con solifenacina o mirabegron solos. Puede ser más beneficioso agregar mirabegron a solifenacina 5 mg, en lugar de aumentar la solifenacina a 10 mg 7.Sin embargo, el factor limitante de esta terapia es su costo.
*En pacientes donde las medidas conductuales pueden ser difíciles de realizar, la medicación puede ser dada como primera línea de tratamiento 7.
Terapias avanzadas
Estos tratamientos de tercera línea, son invasivos, más caros, sin ser 100% efectivos. Son reservados en los casos VHA refractaria al tratamiento conductual y con al menos una medicación. Esto incluye la neuromodulación sacra, la inyección de toxina botulínica intravesical.
TOXINA BOTULINICA INTRAVESICAL
La eficacia de la toxina botulínica A se ha demostrado con una mejora estadísticamente significativa del 60 % en los síntomas. Actualmente, 100 unidades de toxina botulínica A (onabotA; BOTOX®) disueltas en 10 ml de solución salina se inyecta en 20 puntos de la pared de la vejiga por encima del trígono 10.
Se aplica habitualmente en quirófano bajo anestesia. Su efecto es transitorio, por lo cual muchas veces se requiere repetir la inyeccion.
NEUROMODULACION SACRA (NMS)
La neuromodulación sacra (NMS) se refiere a la colocación de un dispositivo percutáneo que a través de un electrodo estimula, neuromodulando, las raíces nerviosas S3. La colocación del neuromodulador requiere una etapa de prueba, y se implanta un dispositivo permanente si hay una mejoría de los síntomas > 50 %. Es un procedimiento invasivo que requiere ser realizado en quirofano, con anestesia general. Además de ser costoso,
El estimulador es un pequeño generador de impulsos eléctricos, aproximadamente del mismo tamaño que un marcapasos cardíaco, y por lo general se implanta en el cuadrante superior externo de la nalga. Las complicaciones más comunes informadas son dolor en el sitio del implante o en el sitio del cable (25%), migración del cable (16%), disfunción intestinal (6%) y necesidad de explantación (9%) 10.

Fig. 1 Consenso de Piso Pelvico. Fasgo 2023
Bibliografia
- Haylen BT, Freeman RM, Lee J, Swift SE, Cosson M, Deprest J, et International Urogynecological Association (IUGA)/International Continence Society (ICS) joint terminology and classification of the complications related to native tissue female pelvic floor surgery. Neurourol Urodyn. abril de 2012;31(4):406–14.
- Blaivas JG, Appell RA, Fantl JA, Leach G, McGuire EJ, Resnick NM, et Definition and classification of urinary incontinence: recommendations of the Urodynamic Society. Neurourol Urodyn. 1997;16(3):149–51.
- Haylen BT, Chetty N, International Continence Society. International Continence Society 2002 terminology report: have urogynecological conditions (diagnoses) been overlooked? Int Urogynecol J Pelvic Floor abril de 2007;18(4):373–7.
- Fitzgerald MP, Brubaker L. Variability of 24-hour voiding diary variables among asymptomatic J Urol. enero de 2003;169(1):207–9.
- Weber AM, Abrams P, Brubaker L, Cundiff G, Davis G, Dmochowski RR, et al. The standardization of terminology for researchers in female pelvic floor Int Urogynecol J Pelvic Floor Dysfunct. 2001;12(3):178–86.
- Haylen BT, de Ridder D, Freeman RM, Swift SE, Berghmans B, Lee J, et al. An International Urogynecological Association (IUGA)/International Continence Society (ICS) joint report on the terminology for female pelvic floor Neurourol Urodyn. 2010;29(1):4–20.
- Lightner DJ, Gomelsky A, Souter L, Vasavada SP. Diagnosis and Treatment of Overactive Bladder (Non-Neurogenic) in Adults: AUA/SUFU Guideline Amendment J Urol. septiembre de 2019;202(3):558–63.
- Cardozo L, Staskin D. Textbook of Female Urology and Urogynecology - Two-Volume Set. CRC Press; 1469 p.
- RAE-ASALE, RAE. «Diccionario de la lengua española» - Edición del Tricentenario. [citado 6 de agosto de 2023]. polidipsia. Disponible en: https://dle.rae.es/polidipsia
- Fontaine C, Papworth E, Pascoe J, Hashim Update on the management of overactive bladder. Ther Adv Urol. 31 de agosto de 2021;13:17562872211039034.
- Swithinbank L, Hashim H, Abrams The effect of fluid intake on urinary symptoms in women. J Urol. julio de 2005;174(1):187–9.
- Robinson D, Cardozo L, Milsom I, Pons ME, Kirby M, Koelbl H, et al. Oestrogens and overactive Neurourol Urodyn. septiembre de 2014;33(7):1086–91.
- Arnold J, McLeod N, Thani-Gasalam R, Rashid P. Overactive bladder syndrome - management and treatment Aust Fam Physician. noviembre de 2012;41(11):878–83.
INCONTINENCIA DE ORINA MIXTA
La Asociación Internacional de Uroginecología y la Sociedad Internacional de Continencia definen a la incontinencia urinaria mixta (IOM) como la presencia de pérdida involuntaria de orina asociada con urgencia y también con esfuerzo, estornudos o tos 1.
La incontinencia urinaria mixta es una condición común pero poco estudiada. Es un reto tanto diagnóstico como terapéutico.
Se estima que más del 30 % de todas las mujeres con incontinencia sufren de IOM causando un impacto negativo en la calidad de vida, significativamente mayor, que la IOE y la IOU por separado 2, 3.
Las mujeres con IOM tienen generalmente síntomas mas severos y responden menos al tratamiento que las pacientes con un solo tipo de IO.
Diagnóstico
El diagnóstico es principalmente clínico. Comienza con el interrogatorio que debe incluir detalles del tipo, momento y la gravedad de la IO. La historia debe permitir clasificar la IO en incontinencia urinaria de esfuerzo (IOE), incontinencia urinaria de urgencia (IOU) o incontinencia urinaria mixta (IOM).
La utilización de cuestionarios validados contribuye al correcto diagnóstico de esta condición.
Los métodos complementarios sugeridos para la mejor evaluación de la IOM son el diario miccional y el EUD.
Tratamiento:
A todos los pacientes debería ofrecerse primero terapia conductual y médica inicial porque estas intervenciones son de bajo riesgo y pueden brindar suficiente alivio de los síntomas para evitar la necesidad de una cirugía, aunque al ser problemas de calidad de vida, es la paciente, acompañada por el consejo médico, quien debe decidir que tratar primero.
Manejo conservador
Incluye rehabilitación de piso pélvico y reeducación vesical.
La evidencia específica para IOM es limitada, una revisión de Cochrane, muestra que las mujeres con cualquier tipo de incontinencia urinaria que se habían sometido a ejercicios de rehabilitación de los músculos del piso pélvico, tenían significativamente más probabilidades de informar la curación 6. También comparó diferentes enfoques para la administración del entrenamiento.
Se debería recomendar entrenamiento intensivo supervisado, con una duración mínima de 3 meses, como tratamiento de primera línea a mujeres con incontinencia urinaria de esfuerzo o incontinencia urinaria mixta. Los programas de EMPP deben ser lo más intensivos posible. (Nivel de recomendación A)
Tratamiento farmacológico
Muchos ECA incluyen pacientes con IOM con síntomas predominantes de IOE o IOU, pero pocos informan los resultados por separado para aquellos con IOM en comparación con los grupos de IOE pura o IOU.
Se recomienda ofrecer fármacos antimuscarínicos a pacientes con incontinencia urinaria mixta con predominio de urgencia. (Nivel de recomendación A)
Tratamiento quirúrgico
Las mujeres con IOM tienen menos probabilidades de curarse de su incontinencia de esfuerzo mediante cirugía que las mujeres con IOE sola. (Nivel de evidencia 1c) . La respuesta de los síntomas de urgencia preexistentes a la cirugía de IOE es impredecible y los síntomas pueden mejorar o empeorar.
Se debe advertir a los pacientes con incontinencia urinaria mixta que la cirugía tiene menos probabilidades de éxito que la cirugía en pacientes con incontinencia urinaria de esfuerzo sola.
Si decidimos indicar el tratamiento quirúrgico debemos tener en cuenta que tipo de sling mediouretral usar 6.
En una paciente con IOM que va a operarse, se podría elegir un TOT sobre un TVT, dado que el TVT tiene mayor tasa de riesgo de ser obstructivo, y esa obstrucción podría producir más urgencia urinaria. Pero la realidad no hay estudios que demuestran que es mejor, y la elección del sling medio uretral debería basarse en las características de la IOE y la paciente, dado que la IOM puede mejorar, quedar igual o empeorar. Se necesita informar a la paciente sobre este riesgo.
Bibliografía:
- Haylen BT, de Ridder D, Freeman RM, et An International Urogynecological Association (IUGA) / International Continence Society (ICS) joint report on the terminology for female pelvic floor dysfunction. Neurourol Urodyn. 2010;19:4–20.
- Gomelsky A, Dmochowski Treatment of mixed urinary incontinence in women. Curr Opin Obstet Gynecol. 2011;23:371–5
- Minassian VA, Stewart WF, Wood Urinary incontinence in women: variation in prevalence estimates and risk factors. Obstet Gynecol. 2008;111:324–31.
- Yao J, Tse Twenty-five years of the MIDURETHRAL sling: Lessons learned. International Neurourology Journal. 2022;26(2):102–10.
- Resnick Geriatric incontinence. Urolog. Clin. North Am. 23(1), 55–74 (1996).
- Todhunter-Brown A, Hazelton C, Campbell P, Elders A, Hagen S, McClurg Conservative interventions for treating urinary incontinence in women: an overview of Cochrane systematic reviews. Cochrane Database of Systematic Reviews. September 2022 .
- Samina Tahseen 1, Peter Reid Effect of transobturator tape on overactive bladder symptoms and urge urinary incontinence in women with mixed urinary incontinence, Obstet 2009 Mar.
- Sung VW, Borello-France D, Newman DK, et al.Effect of Behavioral and Pelvic Floor Muscle Therapy Combined With Surgery vs Surgery Alone on Incontinence Symptoms Among Women With Mixed Urinary Incontinence: The ESTEEM Randomized Clinical JAMA 2019;322:1066–76.
- Salih Polat , Tarik Yonguc y col. Effects of the transobturator tape procedure on overactive bladder symptoms and quality of life: a prospective study . Int Braz J 2019 Nov-Dec
- Paick JS, Oh SJ, Kim SW, Ku Tension-free vaginal tape, suprapubic arc sling, and transobturator tape in the treatment of mixed urinary incontinence in women. Int Urogynecol J Pelvic Floor Dysfunct. 2008;19:123–9.
- Nambiar, K. et al. European Association of Urology Guidelines on the Diagnosis and Management of Female Non-neurogenic Lower Urinary Tract Symptoms. Part 1: Diagnostics, Overactive Bladder, Stress Urinary Incontinence, and Mixed Urinary Incontinence. European Urology, Vol. 82 Nr. 1 Páginas: 49 - 59. 2022
MÉTODOS COMPLEMENTARIOS DE DIAGNOSTICO
Los métodos complementarios en Uroginecología, son herramientas útiles que ayudan a tomar decisiones en determinadas situaciones en las que el interrogatorio y el examen físico no permiten arribar a un diagnóstico.
Los métodos complementarios con los que contamos son:
Estudio Urodinamico (EUD)
Un EUD multicanal es un estudio funcional del tracto urinario bajo que consta de dos partes: la cistometría de llenado, que nos aporta datos como la sensibilidad, la acomodación (que es la capacidad de la vejiga de llenarse a baja presión), la capacidad vesical y la incontinencia de orina (mediante la realización de test de esfuerzo durante el llenado) y la presencia o no de CID (contracciones involuntarias del detrusor), cuya aparición nos podría revelar información sobre la hiperactividad del detrusor. La segunda parte, denominada fase de vaciado o estudio de flujo/presión, nos permite ver la actividad del detrusor en el momento de la micción.
Las actuales indicaciones para solicitar EUD IOE previo a la cirugía con sintomas asociados IOU sin respuesta al tratamiento medico
IO RECURRENTE QUIRURGICA
Disfunción miccional Trastornos neurológicos
Resonancia magnetica nuclear (RMN)
La indicación de la utilización de RMN en la evaluación de la incontinencia urinaria y disfunciones del piso pélvico se basa principalmente en la observación de que algunos pacientes presentan síntomas aislados de un solo compartimiento pero podrían presentar defectos asociados en los demás compartimientos .
Existe un acuerdo general en que la RMN del piso pélvico debe abarcar imágenes de RM estáticas y dinámicas. Las imágenes estáticas visualizan la anatomía del suelo pélvico y los defectos de las estructuras de soporte, mientras que las imágenes de RM dinámicas visualizan la movilidad de los órganos pélvicos, la debilidad del suelo pélvico, el prolapso de órganos pélvicos (POP) y los defectos compartimentales asociados.
Puede ser de beneficio particular:
- Cuando la evaluación clínica es limitada( prolapso recurrente, enteroceles, disfunción defecatoria (anismo), obstrucción rectal .
- Cuando existe una Discordancia entre la evaluación clínica y los síntomas del paciente
Videoefecograma (VDG) :
El videodefecograma es un estudio radiológico contrastado que nos permite ver la función del recto y su interacción con los músculos del piso de la pelvis durante la defecación.
Debe realizarse con distensión rectal usando un enema y un contraste via oral para visualizar las asas de intestino delgado.
El VDG tiene una alta sensibilidad para la evaluación de pacientes con trastornos defecatorios, como puede ser la constipación tipo outlet (obstructiva), donde existe una contracción paradojal del elevador del ano. También es de utilidad para evaluar enterocele o intususcepción.
Evaluación mediante ultrasonido Ecografia transvaginal
Se sugiere como parte de la valoración prequirúrgica.
- Para excluir patologías uterinas antes de realizar una cirugía conservadora de útero
- Para evaluar la longitud del cuello uterino o la relación entre el cuerpo uterino y el cuello uterino (el alargamiento puede provocar síntomas persistentes)
- Para excluir patologías pélvicas extrauterinas
Ecografia vesical
La ecografía vesical es el método de elección para la evaluación del residuo post miccional (RPM) en la práctica clínica, principalmente por ser no invasivo . Es fundamental realizarlo inmediatamente luego de la micción a capacidad cistométrica efectiva (deseo miccional normal) 200/250 ml.
No hay acuerdo sobre el volumen de orina que puede considerarse normal después de la micción. Las pautas de FIGO Group, junto con otras recomendaciones, aconsejan que los volúmenes superiores a 150 ml debe considerarse como anormal o residuo >30% del volumen orinado
Ecografia transperineal
Es una ecografía que se realiza colocando un transductor o sonda ecográfica en el periné. Permite visualizar la vejiga, uretra, vagina, cuello uterino, útero, periné, canal anal y músculos del suelo pélvico.
El abordaje translabial/transperineal supera las limitaciones de las técnicas endovaginales y transrectales proporcionando una mínima presión sobre las estructuras locales y es menos probable que altere la anatomía circundante.
Se pueden evaluar las siguientes anomalías del suelo pélvico/secuelas quirúrgicas:
- Trauma (lesión/daño) del músculo elevador del ano .
- Distensibilidad excesiva del músculo puborrectal y del hiato del
- Patologías del compartimento vaginal anterior como diverticulos
- Tumores vesicales
- Mallas vaginales y slings medio uretrales altamente ecogénicas fácilmente identificables en el plano coronal y axial.
Ecografia endoanal
La ecografía endoanal es ampliamente utilizada ya que es la prueba con mayor más sensibilidad para evaluar defectos del esfínter o cambios estructurales. (83 a 100 % sensibilidad y especificidad para desgarros del esfinter anal)
Puede identificar el espesor y las deformidades estructurales del esfínter anal externo e interno y es eficaz en la detección de lesiones de la pared rectal y músculo puborrectal.
Los hallazgos de la ecografía endoanal para una lesión del esfínter anal suelen asociarse a trastornos funcionales observados en la manometría anorrectal. Los defectos EAE se detectan con una precisión extremadamente alta con esta metodología. (gold standard)
Manometria anorectal
La manometría anorectal y las pruebas sensoriales rectales son efectivas en determinar la función y sensorialidad del esfínter anal externo e interno y anormalidades rectales tales como la incontinencia fecal o trastornos de evacuación .
Los pacientes con Incontinencia anal tienen baja presión del esfínter anal o disminución de las sensación rectal.
Está indicada en la evaluación de incontinencia anal, constipacion, dolor anorrectal y en trastornos defecatorios funcionales .
Test de expulsión del balón intrarectal
El test de expulsión de balón es una prueba sencilla para evaluar la capacidad de expulsión de las heces. Permite detectar a pacientes con constipación tipo outlet u obstructiva. Es una prueba fácil de aplicar y disponible para evaluación en consultorio (mediante el pujo debe lograr la expulsión de un balón con 50 cc de agua antes de un minuto en condiciones normales). Presenta una sensibilidad de 88%, especificidad de 89%, valor de predicción negativa de 97% y valor de predicción positiva de 67% para descartar anismo (trastorno funcional en el que el se produce contracción del haz puborectal, en lugar de su relajación en el momento de la defecación).
Se puede utilizar en pacientes que refieren síntomas obstructivos y presentan defectos del compartimiento posterior previo a la cirugía de un rectocele. En casos de test positivo se podría proseguir con la cirugía y en casos de test de balón negativo se recomienda complementar con otros estudios (ej manomentria anorectal/videodefecografia).
Bibliografia
- Martin J L Williams K S Sutton A J et al. Systematic review and meta-analysis of methods of diagnostic assessment for urinary incontinence Neurourol Urodyn 2006 25674–683.discussion
- Internacional Continence Society / Standard / Urinary Incontinence in women 2/2020
- American Urogynecologic Society Best Practice Statement: Evaluation and Counseling of Patients With Pelvic Organ Prolapse. Female Pelvic Medicine & Reconstructive Surgery 23(5):p 281-287, 9/10 | DOI: 10.1097/SPV.0000000000000424
- Ridgeway, Beri MD; Weinstein, Milena M. MD; Tunitsky-Bitton, Elena MD. American Urogynecologic Society Best-Practice Statement on Evaluation of Obstructed Defecation. Female Pelvic Medicine & Reconstructive Surgery 24(6):p 383-391, 11/12 2018. | DOI: 10.1097/ SPV.0000000000000635
- Digesu G A, Khullar V, Cardozo L. et al. Overactive bladder symptoms: do we need urodynamics? Neurourol 2003;22:105–108.
- Nager CW, Brubaker L, Litman HJ, et al; Urinary Incontinence Treatment Network. A randomized trial of urodynamic testing before stress-incontinence N Engl J Med. 2012 May 24;366(21):1987-97. doi: 10.1056/NEJMoa1113595. Epub 2012 May 2. PMID: 22551104; PMCID: PMC3386296.
- Committee Opinion No. 603: Evaluation of uncomplicated stress urinary incontinence in women before surgical t Obstet Gynecol. 2014 Jun; 123 ( 6 ) : 1403 - 7 . doi: 10.1097/01.AOG.0000450759.34453.31. PMID: 24848922.
- Urinary incontinence and pelvic organ prolapse in women: management NICE guideline Published: 2 April 2019 Last updated: 24 June 2019 nice.org.uk/guidance/ng123
- Giulio Aniello Santoro, Anna Claudia Colangelo , Imaging modalities for pelvic floor disorder, Ann Laparosc Endosc Surg 2022;7:13 | https://dx.doi.org/10.21037/
- El Sayed RF, Alt CD, Maccioni F, Meissnitzer M, Masselli G, Manganaro L, Vinci V, Weishaupt D; ESUR and ESGAR Pelvic Floor Working Magnetic resonance imaging of pelvic floor dysfunction - joint recommendations of the ESUR and ESGAR Pelvic Floor Working Group. Eur Radiol. 2017 May;27(5):2067-2085. doi: 10.1007/s00330-016-4471-7. Epub 2016 Aug 3. PMID: 27488850; PMCID: PMC5374191.
- Kim H, Shim J, Seo Y, Lee C, Chang Y. What Is Fecal Incontinence That Urologists Need to Know? Int Neurourol J. 2021 Mar;25(1):23-33. doi: 10.5213/inj.2040240.120. Epub 2021 Jan 19. PMID: 33504128; PMCID: PMC8022170.
- liss DJ, Mimura T, Berghmans B, et al. Assessment and conservative management of faecal incontinence and quality of life in adults. In: Abrams P, Cardozo L, Wagg A, et al. editors. Incontinence, ICUD ICS, 6th Bristol:International Continence Society; 2017: 1
- Clemons J L, Aguilar V C, Sokol E R. et al. Patient characteristics that are associated with continued pessary use versus surgery after 1 Am J Obstet Gynecol. 2004;191:159–164.
- Sarma S, Ying T, Moore K H. Long-term vaginal ring pessary use: discontinuation rates and adverse BJOG. 2009;116:1715–1721.
- Sitavarin S, Wattanayingcharoenchai R, Manonai et al. The characteristics and satisfaction of the patients using vaginal pessaries. J Med Assoc Thai. 2009;92:744–747.
- Lone F, Thakar R, Sultan A et al. A 5-year prospective study of vaginal pessary use for pelvic organ prolapse. Int J Gynaecol Obstet. 2011;114:56–
- Fleshman JW, et al: Balloon expulsion test facilitates diagnosis of pelvic floor outlet obstructiondue to nonrelaxing puborectalis Dis Colon Rectum 1992;35:1019-25
- Rao SS, Ozturk R, Laine Clinical utility of diagnostic tests for constipation in adults: a systematic review. Am J Gastroenterol. 2005;100:1605–1615.
- Jimenez-Cidre MA, Lopez-Fando L, Esteban-Fuertes M, Prieto-Chaparro L, Llorens-Martinez FJ. The 3-day bladder diary is a feasible, reliable and valid tool to evaluate the lower urinary tract symptoms in women. Neurourol Urodyn. 2015 Feb;34(2):128-32. doi: 10.1002/nau.22530. Epub 2013 Nov 22. PMID: 24264859.
- van Gruting IM, Stankiewicz A, Thakar R, et al. Imaging modalities for the detection of posterior pelvic floor disorders in women with obstructed defaecation syndrome. Cochrane Database Syst Rev 2021;9:CD011
- Faecal incontinence in adults: management Clinical guideline Published: 27 June 2007 nice.org.uk/guidance/cg49
- Carrington EV, Scott SM, Bharucha A, Mion F, Remes-Troche JM, Malcolm A, Heinrich H, Fox M, Rao SS; International Anorectal Physiology Working Group and the International Working Group for Disorders of Gastrointestinal Motility and Expert consensus document: Advances in the evaluation of anorectal function. Nat Rev Gastroenterol Hepatol. 2018 May;15(5):309-323. doi: 10.1038/nrgastro.2018.27. Epub 2018 Apr 11. PMID: 29636555; PMCID: PMC6028941.
- Kwakye G, Maguire LH. Anorectal Physiology Testing for Prolapse-What Tests are Necessary? Clin Colon Rectal Surg. 2021 Jan;34(1):15-21. doi: 10.1055/s-0040-1714246. Epub 2020 Sep 4. PMID: 33536845; PMCID: PMC7843946.
REHABILITACION DE PISO PÉLVICO
El abordaje de las disfunciones del suelo pélvico y aquellas relacionadas con la salud pelviperineal desde la fisioterapia, incluye una serie de procedimientos dirigidos al mantenimiento y mejoría de la musculatura perineal y capacidad funcional con el objetivo de mejorar o conseguir una continencia urinaria y fecal, una correcta estática pelviana, un periodo obstétrico saludable, una sexualidad no dolorosa y satisfactoria así como mejorar la vascularización local, disminuir y aliviar el dolor y en especial mejorar la calidad de vida de quienes las padecen. 1,3
Anatómicamente existe una estrecha relación de la función miccional, sexual y defecatoria con el sistema miofascial y por lo tanto la función de la musculatura del piso pelviano en el soporte de los órganos pélvicos es clara. Los avances de estudios funcionales, como la urodinamia y la defecografía han permitido también valorar que la adecuada coordinación de la musculatura del piso pelviano (MPP) es fundamental en los procesos evacuatorios, de continencia y en la función sexual. El conocimiento del papel que juega el suelo pélvico en los mecanismos de la continencia, como elementos
de sostén de la unión uretrocervical, su implicancia en el sistema esfinteriano estriado, así como las alteraciones neurológicas que conlleva a las disfunciones severas del mismo, ha conseguido que se retome con gran interés aquellas técnicas que llevan a restablecer el estado de normofuncionalidad de estas estructuras como forma de tratamiento de las patologías secundarias a dichas alteraciones: incontinencia urinaria de esfuerzo, de urgencia, mixta, disfunciones sexuales, patologías ginecológicas, obstétricas y colo- proctológicas 2 .
Las técnicas de rehabilitación del suelo pélvico como tratamiento de la incontinencia urinaria femenina de esfuerzo (IOE) se vienen imponiendo en estos últimos años después de que el ginecólogo Arnol Kegel demostrara en 1950 la estrecha relación que existia entre los escapes de orina y la hipotonía o debilidad de la musculatura perineal, desapareciendo o mejorando notablemente los síntomas cuando se practicaban ejercicios de refuerzo de estas estructuras 4.
La rehabilitación es una intervención no invasiva y segura que puede mejorar significativamente la calidad de vida de las personas con incontinencia urinaria. Esta terapia puede incluir ejercicios de fortalecimiento del MPP, reeducación vesical y tratamiento conductual entre otros 5.
Embarazo, parto y posparto
El embarazo y el parto son procesos fisiológicos que generan cambios importantes en el cuerpo de la mujer afectando no sólo a los sistemas cardiovascular, endocrino y renal, sino también al sistema músculoesquelético 6. El periné y el suelo pélvico pueden debilitarse y lesionarse durante el embarazo y el parto, predisponiendo a la mujer a sufrir disfunciones de suelo pélvico en esta etapa de su vida. El estiramiento y la rotura de nervios periféricos, del tejido conectivo y de los músculos pueden ocasionar incontinencia urinaria y fecal, prolapsos de órganos pélvicos, alteraciones sensoriales y de vaciado del tracto urinario inferior, disfunción defecatoria, disfunción sexual y síndromes dolorosos crónicos 7, 8. El mayor factor de riesgo para las disfunciones del suelo pélvico postparto son las disfunciones perineales presentes antes del embarazo, aunque el parto instrumentado con fórceps y las lesiones perineales de 3° y 4° constituyen factores de riesgo independientes 9.
Además, se han descrito otros factores de riesgo como el aumento de peso durante el embarazo, el tiempo de duración del parto, el peso del recién nacido, la episiotomía o la analgesia epidural 10. Aproximadamente el 50 % de las mujeres pierden parte de la función de sostén del suelo pélvico debido al parto. Recientes estudios mediante ecografía y resonancia magnética sugieren una prevalencia de lesiones en la musculatura del suelo pélvico como la avulsión del músculo elevador del ano, cuya prevalencia se estima en torno al 20-26 % 11. Por otro lado, las pacientes que presentaron lesiones del esfínter anal (oasis) tendrán mayor riesgo de sufrir disfunciones anorectales a corto y largo plazo (lesiones perineales obstétricas de 3° y 4° grado) 12 .
Cerca de la mitad de las mujeres embarazadas experimentan incontinencia urinaria. La incontinencia urinaria de esfuerzo es la más común durante el embarazo, aumentando rápidamente durante el segundo trimestre, afectando a alrededor de un 31 % de mujeres nulíparas y a un 42 % de mujeres tras el parto. Una de cada 3 mujeres refieren incontinencia urinaria tras el parto, y aunque esto mejora en torno al año para muchas se convierte en persistente a largo plazo 13.
Tratamiento
El entrenamiento de la musculatura del piso pélvico (EMPP) es una importante herramienta para prevenir las disfunciones del suelo pélvico durante el embarazo y el postparto. La contracción del suelo pélvico produce una elevación de la uretra, la vagina y el recto, estabilizando al suelo pélvico y la resistencia a los movimientos de descenso del mismo. El entrenamiento de la musculatura del suelo pélvico puede reducir el riesgo de incontinencia urinaria tanto al final del embarazo (> 34 semanas) como en el postparto (< 12 semanas tras el parto) 15.
Para las mujeres continentes, el EMPP se recomienda para prevenir las pérdidas de orina, mientras que las mujeres con síntomas tanto en el embarazo como en el postparto, deben ser derivadas a un fisioterapeuta experto en suelo pélvico para recibir tratamiento y supervisión de los ejercicios 16.
El fisioterapeuta de suelo pélvico asesorará a la paciente sobre la recuperación del suelo pélvico, la gestión de cargas y presiones a nivel abdominal y la evaluación de la fuerza para establecer el momento de regresar a la actividad física. Es necesario considerar factores adicionales en esta evaluación como el peso, el estado físico, la respiración, el estado psicológico, la presencia de diástasis de rectos abdominales, la lactancia materna o el sobreentrenamiento, así como la posibilidad de todo lo que genere aumento de la presión intra abdominal (PIA) 14.
Incontinencia de orina de esfuerzo
El objetivo principal es abordar los factores de riesgo modificables que puedan generar un aumento de PIA, mejorar el trofismo y tono de la MSP.
La fisioterapia es, un elemento importante del tratamiento conservador de la incontinencia urinaria (IO); considerándose la primera línea del abordaje 17.
El entrenamiento muscular del suelo pélvico, fortalece la musculatura e inhibe la contracción del detrusor 19. La guía NICE de incontinencia urinaria, establece como
directrices para un entrenamiento adecuado que se realice un mínimo de 3 meses, con una ejecución de 8 repeticiones y durante 3 veces al día 20. Con su práctica, el grosor muscular aumenta, disminuye el área hiatal, mejora la longitud de la musculatura acortada y mejora el soporte de la pared vaginal anterior 21.
Se trabajan técnicas para disminuir la presión abdominal, se entrena la coordinación y sincronismo entre el aumento de la PIA y contracción perineal, creando un efecto de defensa ante la pérdida de orina.
Incontinencia de orina por urgencia
El objetivo del tratamiento es reducir las contracciones involuntarias del detrusor durante la fase de llenado. Para logarlo es necesario abordar todos los factores de riesgos modificables. La pérdida de peso y la actividad física leve-moderada reducen el riesgo de IOU. La utilizacion de la neuromodulación del tibial posterior (PTNS) ha mostrado ser efectiva 24. Aunque su mecanismo no está claro, se ha comprobado que genera una inhibición de las vías inhibitorias aferentes, obteniendo efectos neuromoduladores sensoriales, tales como tono inhibitorio creciente, conciencia decreciente de estimulos anormales, y reorganización del sistema neuronal 25. En una revisión realizada en 2013, se concluye que consigue una reducción de las contracciones involuntarias del detrusor 26.
Bibliografía
- Fuentes the role of a physiotherapist in the pelvic floor. Rev. med. clin. condes - 2013; 24(2) 305-312]
- Hay-Smith Esc, Bo K, Berghmans LMC, Hendrikg Hjm, de Bier A, van Pelvis floor muscle trainig for urinary iii . Actas Urológicas Españolas versión impresa ISSN 0210-4806
- Actas Urol Esp vol.31 no.7 jul./ago. 2007 Treatment of the dysfunction of the pelvic floor- Pena Outeiriño M., Rodríguez Pérez A.J., Villodres Duarte A., Mármol Navarro S., Lozano Blasco J.M. Servicio de Urología. Unidad de Neurourología y Uroginecología. Hospital Universitario Virgen del Rocío. Sevilla.
- Effects of inner muscle resistance exercise on stress urinary incontinence: a randomized clinical controlled trial- Phys- Ther. Sci. 33: 748-752, 2021. The Journal of Physical Therapy Scince.- Lin Lyu1, 2), Chunying Hu3), Miao Ye3), Cong Chen3), Ming Huo, RPT, PhD4)*, Shinichiro Murakami, RPT, PhD4), Ko Onoda, RPT, PhD5), Hitoshi Maruyama, RPT, PhD6)
- Vanessa Uclés Villalobos, María Félix Sánchez Solera. Revista Clínica de la Escuela de Medicina UCR – HSJD Año 2015 Vol 5 No TEMA 3 -2017: Rehabilitación del Piso Pélvico- ISSN 2215-2741.
- Casagrande D, Gugala Z, Clark SM, Lindsey RW. Low Back Pain and Pelvic Girdle Pain in J Am Acad Orthop Surg. 2015 Sep;23(9):539-49. doi:10.5435/jaaos-D-14-00248. Epub 2015 Aug 13. pmid: 26271756.
- Morkved S, Bo Eff ect of pelvic fl oor muscle training durng pregnancy and aft er childbirth on prevention and treatment of urinary incontinence: a systematic review. Br J Sports Med. 2014 Feb;48(4):299-310. doi: 10.1136/bjsports2012-091758. Epub 2013 Jan 30. pmid: 23365417.
- Schreiner L, Crivelatti I, de Oliveira JM, Nygaard CC, Dos Santos TG. Systematicreview of pelvic fl oor interventions during Int J Gynaecol Obstet. 2018 Oct;143(1):10-18. doi: 10.1002/ ijgo.12513. Epub 2018 May 18. pmid: 29705985.
- Lawson S, Sacks Pelvic Floor Physical Th erapy and Women’s Health Promotion. J Midwifery Womens Health. 2018Jul;63(4):410-417. doi: 10.1111/jmwh.12736. Epub 2018 May 19. pmid: 29778086.
- Bozkurt M, Yumru AE, Şahin Pelvic fl oor dysfunction, and eff ects of pregnancy and mode of delivery on pelvic fl oor. Taiwan JObstet Gynecol. 2014Dec;53(4):452-8. doi: 10.1016/ j.tjog.2014.08.001. pmid: 25510682.
- Handa VL, Blomquist JL, Roem J, Munoz A, Dietz HP. Pelvic Floor Disorders Aft er Obstetric Avulsion of the Levator Ani Female Pelvic Med Reconstr Surg. 2019 Jan/Feb;25(1):3-7. doi: 10.1097/spv.0000000000000644. pmid: 30285979.
- Meekins AR, Siddiqui Diagnosis and Management of Postpartum PelvicFloor Disorders. Obstet Gynecol Clin North Am. 2020 Sep;47(3):477-486. doi:10.1016/j.ogc.2020.05.002. pmid: 32762932.
- Woodley, SJ, Hay-Smith EJC. Narrative review of pelvic fl oor muscle training for childbearing women-why, when, what, and Int Urogynecol J. 2021 Jul;32(7):1977-1988. doi: 10.1007/ s00192-021-04804-z. Epub 2021 May 5. pmid:33950309.
- Goom T, Donnelly G, Brockwell Returning to running postnatal – guideline for medical, health and fi tness professionals managing this population. Available:https://www.absolute.physio/wp- content/uploads/2019/09/returning-to-runningpostnatal-guidelines.pdf.
- Schreiner L, Crivelatti I, de Oliveira JM, Nygaard CC, Dos Santos Systematic review of pelvic fl oor interventions during pregnancy. Int J Gynaecol Obstet. 2018 Oct;143(1):10-18. doi: 10.1002/ ijgo.12513. Epub 2018 May 18. pmid: 29705985.
- Woodley, SJ, Hay-Smith EJC. Narrative review of pelvic fl oor muscle training for childbearing women-why, when, what, and how. Int Urogynecol J. 2021Jul;32(7):1977-1988. doi: 10.1007/ s00192- 021-04804-z. Epub 2021 May 5. pmid: 33950309.
- Mazur-Bialy AI, Kołomańska-Bogucka D, Nowakowski C, Tim S. Urinary incontinence in women: Modern methods of physiotherapy as a support for surgical treatment or independent J Clin Med. 2020;9
- Dumoulin C, Cacciari LP, Hay-Smith EJC. Pelvic fl oor muscle training versus no treatment, or inactive control treatments, for urinary incontinence in Cochrane Database Syst Rev. 2018 Oct 4;2018
- Bendahan-Barchilon G, Fortuny M, Garolera D, Gras R, Narbona P, Vila MA. Recomanacions per a l’ús de bolquers en la incontinencia urinaria: guies de practica clínica i material Institut Catala de la Salut. Institut Catala de la Salut; 2002.
- Aoki Y, Brown HW, Brubaker L, Cornu JN, Daly JO, Cartwright Urinary incontinence in women.
- Nat Rev Dis Prim. 2017 Jul 6;3:17042.,19 Wood LN, Anger JT. Urinary incontinence in women. bmj. 2014;349. .
- Díaz Mohedo E, Medrano Sánchez EM, Suárez Serrano Guía de práctica clínica para fi sioterapeutas en la incontinencia urinaria femenina. Vol. 1, Colegio Profesional de Fisioterapeutas de Andalucía. 2013. 1-92 p
- Hoff Brakken I, Majida M, Engh ME, Bo Morphological changes aft er pelvic fl oor muscle training measured by 3-dimensional ultrasonography: a randomized controlled trial. Obstet Gynecol. 2010 Feb;115(2 Pt 1):317-24.
- Potts JM, Payne CK. Urinary Urgency in the Elderly. Gerontology.2018;64(6):541-50 Nygaard IE, Shaw JM. Physical activity and the pelvic fl oor. Am J Obstet Gynecol. 2016 Feb;214(2):164-71
- Yoong W, Ridout AE, Damodaram M, Dadswell R. Neuromodulative treatment with percutaneous tibial nerve stimulation for intractable detrusor instability:Outcomes following a shortened 6-week protocol. bju 2010;106(11):1673-6
- Tubaro A, Puccini F, De Nunzio Th e management of overactive bladder: percutaneous tibial nerve stimulation, sacral nerve stimulation, or botulinum toxin? Curr Opin Urol. 2015 Jul;25(4):305-10
- Gaziev G, Topazio L, Iacovelli V, Asimakopoulos A, Di Santo A, De Nunzio C, et Percutaneous tibial nerve stimulation (ptns) effi cacy in the treatment of lower urinary tract dysfunctions: A systematic review. bmc Urol. 2013;13.
- Lawson S, Sacks A. Pelvic Floor Physical Therapy and Women’s Health Promotion. J Midwifery Womens Health. 2018 Jul;63(4):410-417. doi: 10.1111/jmwh.12736. Epub 2018 May 19. pmid:
PROLAPSO ANTERIOR Y APICAL
Definición
El prolapso de órganos pélvicos (POP) se define como el descenso de las paredes vaginales anterior, posterior, el útero y/o cérvix o la cúpula vaginal (en pacientes histerectomizadas)1.
Los órganos involucrados en dicho descenso pueden incluir al útero, la uretra y vejiga, el recto, el colon sigmoide y el intestino delgado.
Este desplazamiento se produce como consecuencia del fallo de las estructuras de soporte y puede alcanzar diferentes grados 2.
El origen del POP es multifactorial y no del todo conocido, entre sus causas más importantes podemos incluir algunos hechos fundamentales que suceden en la vida de
la mujer: embarazo y parto, menopausia, y todas aquellas que generen un aumento crónico de la presión abdominal o debilitamiento del piso de la pelvis (obesidad, tos crónica, constipación) y factores genéticos, entre otros 3.
El POP afecta aproximadamente al 50% de las mujeres mayores de 50 años. Se calcula que 1 de cada 5 mujeres requerirán tratamiento quirúrgico 4.
Dada la expectativa de vida en la actualidad (aproximadamente 80 años para las mujeres), se calcula que requerirán tratamiento quirúrgico por POP un 11-12% de ellas, con una tasa de reintervención de hasta el 29% 5.
Clasificación
Se recomienda la clasificación POP-Q (Pelvic Organ Prolapse Quantification System - Sistema de cuantificación del prolapso de órganos pelvianos), que ha sido avalada por la mayoría de las sociedades cientificas tanto para su utilización clínica como para investigación 1, 6, 7.
Según el compartimiento involucrado podemos clasificarlo en POP Anterior, Apical y Posterior. Prolapso Anterior y Apical
El Prolapso Anterior se define como el descenso de la pared vaginal anterior desde cualquier punto que se encuentre por encima de la unión uretrovesical (aproximadamente a 3 cm proximal al meato uretral) o 3 cm por encima del himen2.
El órgano más frecuentemente involucrado es la vejiga, aunque raramente puede producirse un enterocele anterior (intestino delgado).
En los estadíos avanzados (generalmente cuando el prolapso anterior se exterioriza 3 cm por debajo del plano del himen, debemos tener en cuenta la fuerte asociación con un prolapso apical coexistente 8. Por este motivo los estudiaremos en forma conjunta.
El Prolapso Apical implica el descenso del útero o la cicatriz de la cúpula vaginal (en pacientes sin útero) desde su ubicación habitual, pudiendo exteriorizarse a través de los genitales externos completamente.
No debemos confundir un prolapso apical, (definido a través del punto D = Sitio de inserción de los ligamentos Uterosacros en la cara posterior del cérvix) con una elongación cervical (donde el punto que lo define será el C = cérvix, estando el cuerpo uterino in situ, o sea el punto D en su lugar habitual) 1.
Estudios múltiples demuestran que cuando el ápex desciende con el compartimiento anterior, la corrección de la pared anterior sin abordar el ápice aumenta el riesgo de prolapso recurrente.
Clínica
Los síntomas del POP son muy variables y afectan en mayor o menor medida la calidad de vida de las mujeres, pudiendo ser totalmente asintomáticos o generar síntomas
realmente invalidantes, que derivan en cuadros de retracción y aislamiento psico-social. Estos dependen fundamentalmente del tipo y estadío del prolapso.
Un dato fundamental es que la necesidad de tratamiento o no, va a depender de la gravedad de los síntomas y la necesidad de la mujer de recibir ese tratamiento, ya que a veces, sobretratar un prolapso asintomático, solo por haberlo encontrado en un examen de rutina, deriva en nuevos síntomas que la paciente no tenía previamente, principalmente cuando se realizan tratamientos quirúrgicos innecesarios.
El síntoma predominante en todos los POP es la “sensación de cuerpo extraño vaginal”. La mujer siente que tiene algo que ocupa lugar dentro de su vagina y le ocasiona disconfort.
Con la progresión de ese POP en el tiempo, puede producirse la exteriorización de bulto por los genitales externos, momento en el cual, las pacientes suelen acudir a la consulta.
Específicamente en el POP apical y anterior, además del bulto, vamos a encontrar síntomas vinculados principalmente al tracto urinario bajo, entre ellos:
- Incontinencia de
- Síntomas de disfunción obstructiva del vaciado vesical (Dificultad para iniciar la micción, chorro lento o en spray, urgencia y frecuencia miccional, nocturia, sensación de vaciado vesical incompleto, residuo postmiccional elevado)
- Infección urinaria
- Vaginitis Flujo patológico.
- Lesiones por decúbito.
- Disconfort . Dispareunia.
- Dolor pélvico crónico. Dolor sacro-lumbar inespecífico.
Diagnostico
El diagnóstico del prolapso de órganos pélvicos es eminentemente clínico.
Dentro de las pruebas altamente recomendadas para el diagnóstico encontramos:
- Adecuado y exhaustivo interrogatorio de los síntomas y afección de la calidad de
- Examen físico y uroginecológico.
- Estadificación del prolapso mediante el sistema POP-Q.
- Cuestionarios de impacto de calidad de
Estudios adicionales, si bien son útiles y necesarios en muchos casos, se recomienda realizarlos individualizando a cada paciente, considerando síntomas, tipo y estadío de prolapso y estrategias terapéuticas. Entre ellos, en el caso del prolapso apical y anterior vamos a considerar:
- Laboratorio: sedimento de orina y Análisis de función renal en estadíos avanzados (por riesgo de obstrucción ureteral)
- Ecografía renal para valorar hidronefrosis en prolapsos estadio IV y vesical con medición de residuo
- Ecografía transperineal
- Urodinamia
Tratamiento del prolapso anterior y apical
El objetivo del tratamiento será restaurar tanto la anatomía como la función urinaria, intestinal y sexual 9.
La decisión sobre el tratamiento debe ser individualizada, teniendo en cuenta diferentes variables, siendo las más importantes: el tipo y estadío del prolapso, la actividad sexual, los factores de riesgo y el deseo y expectativas de la mujer.
El tratamiento del POP puede ser conservador o quirúrgico. El tratamiento quirúrgico se reserva para prolapsos sintomáticos.
Tratamiento conservador Incluye:
- Medidas higiénico-dietéticas y cambios en el estilo de
- Ejercicios musculares de piso pélvico (en estadíos tempranos).
- Dispositivos intravaginales (pesarios).
Los ejercicios musculares de piso pélvico monitoreados por un profesional entrenado, acompañados de modificaciones en el estilo de vida y la aplicación de estrogenoterapia local, son recursos útiles en estadíos I y II sintomáticos, pudiendo lograr una leve retracción del POP y eliminar los síntomas.
Los pesarios vaginales son considerados en la actualidad el Gold Standard en el tratamiento conservador del prolapso de órganos pélvicos, constituyendo un excelente recurso de tratamiento con una tasa de éxito entre el 41 al 74% 10, siendo costo-efectivos, de bajo riesgo, casi exento de complicaciones serias y efectos indeseables. Se recomienda su recambio periodico (3-6 meses) para evaluar el epitelio vaginal y evitar
complicaciones asociadas al uso del mismo que son la leucorrea, la ginecorragia o el encarcelamiento.
Deben ser considerados en aquellas pacientes que no son candidatas para tratamiento quirúrgico, entre las principales indicaciones podemos citar:
- Pacientes jóvenes con maternidad no
- Adultas mayores con
- Contraindicaciones clínicas para tratamiento quirúrgico (alto riesgo).
- No deseo de tratamientos invasivos por parte de la
Tratamiento quirúrgico:
El tratamiento quirúrgico será siempre el tratamiento definitivo del POP.
Muchas cirugías y vías de abordaje han sido descritas a lo largo de la historia. Por cuestiones prácticas, presentaremos sólo las más utilizadas y avaladas en la actualidad.
Lo primero que debemos considerar cuando decidimos una cirugía es elegir entre técnicas reconstructivas o técnicas obliterativas, y ello dependerá del estatus sexual de la paciente presente y futuro. El consentimiento adecuado es muy importante en esta instancia.
Si decidimos utilizar una técnica reconstructiva, deberemos tomar varias decisiones más, entre ellas:
- Abordaje Vaginal o Abdominal?
- Histerectomía o conservación uterina?
- Utilización de dispositivos/mallas o cirugías con tejidos nativos?
Claramente todo este análisis debe ser individualizado teniendo en cuenta su edad, comorbilidades y factores de riesgo, tipo y grado de POP, expectativas y deseos de la paciente. Si bien no debería ser un factor, es una realidad que la comodidad y habilidades aprendidas del cirujano también influye en la toma de decisiones.
En el año 2020, IUGA y AUGS realizaron un informe conjunto sobre las cirugías avaladas y más utilizadas en la actualidad 11.
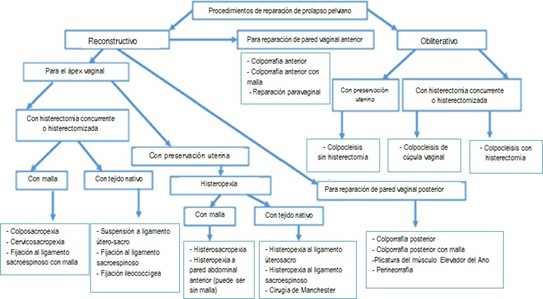
Fig. 2. Tomado de Joint report on terminology for surgical procedures to treat pelvic organ prolapse. Int Urogynecol J. 2020
La evidencia cientifica señala a la COLPOSACROPEXIA ABDOMINAL como gold standard de tratamiento quirúrgico del prolapso apical. Sin embargo, es bien sabido que más del 80% de las cirugías de POP en el mundo se realizan por VÍA VAGINAL.
Lo cierto es que lo ideal es adecuar dicha elección en virtud de las características de las pacientes. No existe consenso acerca de qué cirugía deberíamos elegir en cada escenario pero en términos generales hay bastante acuerdo en elegir el abordaje de la siguiente manera 12:
|
PREFERENTEMENTE VÍA ABDOMINAL |
PREFERENTEMENTE VÍA VAGINAL |
|
Prolapsos apicales avanzados |
Gran componente anterior en el POP |
|
Recurrencias/Fallas quirúrgicas |
Adultas mayores |
|
Dolor vaginal crónico |
Cirugías abdominales y pelvianas previas |
|
Actividades de alto impacto |
Comorbilidades. Riesgo quirúrgico |
|
Pacientes jovenes |
|
|
Vaginas acortadas |
El principal problema que se ha relacionado con la cirugía vaginal clásica con tejidos nativos es la alta tasa de recurrencia y reoperaciones. Las tasas publicadas en la literatura son muy variables, lo
cual dificulta la comparación de los resultados. Si bien históricamente se han descrito bajas tasas de éxito, en el órden del 45%, llama la atención que la tasa de reoperaciones estimada oscila entre el 0.7 y 5.4% 13.
Sin embargo estas consideraciones han sido revisadas en un estudio publicado en 2011, en el cual, cambiando la forma de evaluar el éxito, se dejaron de considerar resultados anatómicos estrictos y se pasó a considerar resultados funcionales y grado de satisfacción de las pacientes. De esta manera se observó que las tasas de éxito para las técnicas clásicas mejoró considerablemente, encontrándose en el órden del 89% 14.
El advenimiento de las mallas vaginales surgió de la necesidad de disminuir las recurrencias y aunque, efectivamente están asociadas a mejores resultados anatómicos en la pared anterior, agrega complicaciones vinculadas a la utilización de la malla.
MALLAS VAGINALES EN EL TRATAMIENTO DEL POP. SITUACIÓN ACTUAL
Desde hace más de 20 años los investigadores han propuesto la utilización de materiales sintéticos para tratar prolapsos de “alto riesgo de recurrencia”, con el objetivo de disminuir las fallas quirúrgicas.
De tal modo el mercado se vió invadido de una gran variedad de mallas vaginales de diferentes
materiales, formas y tamaños, provenientes de la industria, lo que dió lugar a que cirujanos pobremente entrenados en su utilización, comenzaran a colocar mallas vaginales incluso a pacientes que no aplicaban criterios para su colocación. En el año 2010, unas 300.000 mujeres se sometieron a cirugías con malla para tratar su prolapso de órganos pélvicos.
En consecuencia comenzaron a observarse complicaciones, la mayoría de ellas menores y de resolución sencilla. Entre ellas las más prevalentes son las infecciones, hematomas, trastornos de la cicatrización (exposición), dolor transitorio, disconfort sexual, contracción de la malla. Estas complicaciones podemos observarlas entre el 0.6 al 24% de los casos (15-16-17).
Esto ha motivado a la revisión de las mismas por parte de diversos organismos de control, entre ellos citaremos a la FDA. Lo que condujo a que dejaran de comercializarse en muchos lugares del mundo.
Posicionamiento de la Asociación Uroginecológica Argentina (AUGA)
La AUGA, en un comunicado del año 2021 por parte de su presidente, avala el uso de dispositivos transvaginales con malla sintética disponibles en nuestro país en las pacientes que, de acuerdo a la bibliografía y el consenso internacional puedan beneficiarse con las mismas, es decir: las recurrencias y las que tienen alto riesgo de falla. Sin embargo considera que deben ser utilizadas por cirujanos entrenados, preferentemente con alto volumen de cirugías, respetando las indicaciones y sabiendo manejar o eventualmente derivar, las complicaciones (19).
Algunas consideraciones finales:
- Las técnicas más recomendadas en la actualidad para el tratamiento del prolapso apical anterior por vía vaginal son la colposuspensión uterosacral alta o la fijación al ligamento sacroespinoso. Ambas cirugías fueron comparadas en un estudio (OPTIMAL trial) demostrando ser efectivas y equiparables en términos de tasas de éxito y tasas de retratamiento, siendo estas últimas incluso menores que el Gold standard, colposacropexia (CARE trial extendido). Probablemente la elección de una u otra debiera ser considerada según el entrenamiento y comodidad del cirujano. (20)
- Una alternativa a la fijación sacroespinosa clásica, es la suspensión apical bilateral al ligamento Sacroespinoso con dispositivos (Sling apical y suturas montadas en arpones). Ésta es una innovación que debe ser diferenciada de las demás técnicas por vía vaginal, incluso de las mallas vaginales con cuerpo, debido a que plantea diferentes resultados anatómicos esperables y diferentes complicaciones. En pocas palabras es una técnica que aporta simplificación de la técnica quirúrgica mediante disecciones mínimas y facilidad de acceso al espacio mediante un introductor; la suspensión bilateral evita la desviación lateral de la vagina, dejándola en una posición medial y más fisiológica, con menor tiempo quirúrgico y tasa de Estas ventajas, si bien se necesita más evidencia cientifica, han sido estudiadas en un trabajo multicéntrico con participación de autores argentinos.(21)
- La cirugía obliterativa (colpocleisis) debe ser considerada una excelente opción en pacientes de alto riesgo quirúrgico y sin deseo definitivo de vida sexual activa con penetración vaginal, ya que representa una cirugía prácticamente de superficie, con exigua tasa de complicaciones, muy corto tiempo quirúrgico y es altamente resolutiva, con tasas de recurrencia muy bajas y generalmente relacionadas con defectos en la técnica quirúrgica22.
Bibliografía
- Haylen B, de Ridder D, Freeman RM et al. An international urogynecological association (IUGA) / international continence society (ICS) joint report on the terminology for female pelvic floor Neurourol Urodynam 2010; 29: 4-20. (Int Urogynecol J. 2010;21:5-26)
- Abrams P, Cardozo L, Fall M, Griffiths D, Rosier P, Ulmsten U et al. The standardisation of terminology in lower urinary tract function: report from the standardisation sub-committee of the International Continence Neurourol Urodyn 2002; 21: 167-178.
- Lucot JP, Fritel X, Debodinance P, Bader G, Cosson M, Giraudet G, Collinet P, Rubod C, Fernandez H, Fournet S, Lesavre M, Deffieux X, Faivre E, Trichot C, Demoulin G, Jacquetin B, Savary D, Botchorichvili R, Campagne Loiseau S, Salet-Lizee D, Villet R, Gadonneix P, Delporte P, Ferry P, Aucouturier JS, Thirouard Y, de Tayrac R, Fatton B, Wagner L, Nadeau C, Wattiez A, Garbin O, Youssef Azer Akladios C, Thoma V, Baulon Thaveau E, Saussine C, Hermieu JF, Delmas V, Blanc S, Tardif D, Fauconnier A; GROG (groupe de recherche en gynécologie et obstétrique). PROSPERE randomized controlled trial: laparoscopic sacropexy versus vaginal mesh for cystocele POP repair. J Gynecol Obstet Biol Reprod (Paris). 2013 Jun;42(4):334-41. doi: 10.1016/j.jgyn.2013.03.012. Epub 2013 Apr 22.
- Welk, , Carlson, K., Baverstock, R. et al. Canadian Urological Association position statement on the use of transvaginal mesh. Can Urol Assoc J. 2017 Jun; 11(6Suppl2): S105–S107.
- Hwa Choi K, Yuo Hong J. Managemnet of Pelvic Organ Prolapse. Korean J Urol. 2014; 55: 693-702.
- Bump RC, Mattiasson A, Bø K, et al. The standardization of terminology of female pelvic organ prolapse and pelvic floor Am J Obstet Gynecol. 1996;175:10-17.
- Haylen BT, Maher CF, Barber MD, et Erratum to: An International Urogynecological Association (IUGA)/International Continence Society (ICS) joint report on the terminology for female pelvic organ prolapse (POP). IntUrogynecolJ. 2016;27:655-684.
- Rooney K, Kenton K, Mueller ER, FitzGerald MP, Brubaker Advanced anterior vaginal wall prolapse is highly correlated with apical prolapse. Am J Obstet Gynecol. 2006 Dec;195(6):1837-40.
- Maher C., Feiner, B, Baessler, K, Schmid C. Surgical managment of pelvic organ prolapse in women (Review). The Cochrane Library. 2013
- Jeffrey L Vaginal pessary treatment of prolapse and incontinence. This topic last updated: Mar 10, 2014. In: Uptodate, Linda Brubaker, FACOG (Ed), UpToDate, Waltham, MA,2015.
- Developed by the Joint Writing Group of the American Urogynecologic Society and the International Urogynecological Association. Joint report on terminology for surgical procedures to treat pelvic organ prolapse. Int Urogynecol J. 2020 Mar;31(3):429-463.
- Anand, Mallika; Weaver, Amy L.; Fruth, Kristin M.; Gebhart, John B. (2016). Factors Influencing Selection of Vaginal, Open Abdominal, or Robotic Surgery to Treat Apical Vaginal Vault Prolapse. Female Pelvic Medicine & Reconstructive Surgery, 22(4), 236–242.
- Friedman T, Eslick GD, Dietz HP. Risk factors for prolapse recurrence: systematic review and meta-analysis. Int urogynecol J. 2018; 29: 13-21.
- Chmielewski L, Walters MD, Weber AM, et al. Reanalysis of a randomized trial of 3 techniques of anterior colporrhaphy using clinically relevant definitions of Am J Obstet Gynecol 2011;205:69.e1-8.
- Thomas T, Siff L, Jelovsek E, Barber M. Surgical Pain After Transobturator and Retropubic Midurethral Sling Placement. Obstet Gynecol. 2017; 130(1):
- Pesce Current management of stress urinary incontinence. BJU Int 2004; 94 (Suppl 1): 8-13.
- Serati M, Braga A, Athanasiou S, Tommaselli GA, Caccia G, Torella M, Ghezzi F, Salvatore S. Tension-free Vaginal Tape-Obturator for Treatment of Pure Urodynamic Stress Urinary Incontinence: Efficacy and Adverse Effects at 10-year Follow-up. Eur 2017 Apr;71(4):674- 679. doi: 10.1016/j.eururo.2016.08.054. Epub 2016 Sep 3.
- Reclassification of Urogynecologic Surgical Mesh Instrumentation Food and Drug Administration Gastroenterology-Urology Medical Devices Advisory Committee February 26, 2016.
- auga.com
- Matthew Barber, MD, MHS, Obstetrics/Gynecology and Women’s Health Institute, Cleveland Clinic. The OPTIMAL randomized trial. JAMA. 2014;311(10):1023-1034.
- Castro RA, Bortolini MAT, Pascom ALG, Ledesma M, Sardi JJL, Monteiro MVC, Junqueira SP, Fuentes Vaginal Sacrospinous Ligament Fixation Using Tissue Anchoring System Versus a Traditional Technique for Women With Apical Vaginal Prolapse: A Randomized Controlled Trial. Female Pelvic Med Reconstr Surg. 2021 Jan 1;27(1):e215-e222.
- Song X, Zhu L, Ding J, Xu T, Lang J. Long-term follow-up after LeFort colpocleisis: patient satisfaction, regret rate, and pelvic Menopause. 2016 Jun;23(6):621-5.
PROLAPSO DEL COMPARTIMIENTO POSTERIOR
Epidemiologia
No hay correlación entre los síntomas del prolapso posterior y el estadio. Cuando se define por síntomas tiene una baja prevalencia entre un 3 a un 6% y hasta un 50% cuando se basa en el examen vaginal 2,3.
Diagnostico:
El diagnóstico es principalmente clínico. La paciente debe ser examinada en posición de litotomía dorsal y en posición de pie.
Los prolapsos tienden a ser sintomático cuando se extienden más allá del anillo himeneal.
Los síntomas comúnmente asociados con el POP posterior incluyen digitación para defecar, presión pélvica o pesadez, estreñimiento, disfunción sexual, incontinencia fecal y disfunción defecatoria
5,6,7,8,9,10.
Las mujeres cuyos síntomas no concuerdan con los hallazgos del examen o que tienen defectos recurrentes de la pared vaginal posterior también pueden beneficiarse de la evaluación por
imágenes y pruebas complementarias. Las imágenes no se utilizan de forma rutinaria en la evaluación de los defectos de la pared posterior ya que el diagnóstico es principalmente clínico.
El VDG puede ser útil en los defectos de este compartimento, para la valoración del enterocele, rectocele y la intususcepcion rectal asi como también en pacientes con constipación obstructiva, junto con la manometria, sirve para evaluar la contracción paradojal del elevador del ano10.
Tratamiento
El tratamiento quirúrgico debe proponerse en los casos en que el prolapso es sintomático. Se le debe asesorar sobre los posibles resultados con el manejo expectante, las opciones no quirúrgicas (pesario, fisioterapia) y la cirugía.
El objetivo de la reparación de la pared vaginal posterior es corregir el defecto, aliviar los síntomas y restablecer la anatomía y la función sexual.
Hay dos métodos principales de reparación transvaginal del rectocele: la colporrafia posterior tradicional y la reparación sitio específica.
Las mallas transvaginales en esta ubicación no mejora los resultados y se asocia con un mayor riesgo de complicaciones 11,12.
La colporrafia posterior (plicatura de la fascia rectovaginal en la línea media) tiene una tasa de curación anatómica del 76 al 96 %. La reparación sitio específica (identificación de la fascia desinsertada, y reparación posterior del sitio del daño) tiene una tasa de curación anatómica del 82 al 100%13.
Una perineorrafia (reparación de los músculos bulbocavernoso y transverso superficial), cuando está indicada, completa el abordaje vaginal para la reparación de un rectocele. Está demostrado que el hiato genital amplio es un factor de riesgo de recurrencia independiente en las pacientes sometidas a cirugía de patología de piso pélvico 14,15,16,17,18.
Actualmente se desaconseja la miorrafia sistemática de los elevadores del ano.
Bibliografía
- Sarah A. Collins, Michele O’Shea,et al . International Urogynecological Consultation: clinical definition of pelvic organ prolapse International Urogynecology Journal volume 32, pages2011– 2019 (2021)
- Matthew D. Barber & Christopher Maher Epidemiology and outcome assessment of pelvic organ prolapse International Urogynecology Journal 24, pages1783–1790 (2013)Cite this article
- MD Ambre L. Olsen, MD Virginia J. Smith, MD John O. Bergstrom, RN, PhD Joyce C. Colling, MD Amanda L. Clark, et al. Epidemiology of surgically managed pelvic organ prolapse and urinary incontinence Obstetrics & Gynecology Volume 89, Issue 4, April 1997, Pages 501-506
- A L Olsen 1, V J Smith, J O Bergstrom, J C Colling, A L Clark Epidemiology of surgically managed pelvic organ prolapse and urinary Obstet Gynecol1997 Apr;89(4):501-6. doi: 10.1016/S0029-7844(97)00058-6
- Steven E Swift 1, Susan B Tate, Joyce Nicholas. Correlation of symptoms with degree of pelvic organ support in a general population of women: what is pelvic organ prolapse? Am J Obstet 2003 Aug;189(2):372-7; discussion 377-9. doi: 10.1067/s0002-9378(03)00698-7.
- R M Ellerkmann 1, G W Cundiff, C F Melick, M A Nihira, K Leffler, A E Bent. Correlation of symptoms with location and severity of pelvic organ Am J Obstet Gynecol 2001 Dec;185(6):1332-7; discussion 1337-8. doi: 10.1067/mob.2001.119078
- A M Weber 1, M D Walters, L A Ballard, D L Booher, M R Piedmonte. Posterior vaginal prolapse and bowel function. Am J Obstet Gynecol 1998 Dec;179(6 Pt 1):1446-9; discussion 1449-50. doi: 1016/s0002-9378(98)70008-0.
- S L Jackson 1, A M Weber, T L Hull, A R Mitchinson, M D Walters Fecal incontinence in women with urinary incontinence and pelvic organ prolapse. Obstet Gynecol 1997 Mar;89(3):423-7. doi: 1016/S0029-7844(96)00499-1.
- Catherine Matthews Nichols 1, Edward J Gill, Tuc Nguyen, Matthew D Barber, W Glenn Hurt. Anal sphincter injury in women with pelvic floor disorders. Obstet Gynecol 2004 Oct;104(4):690-6. doi: 1097/01.AOG.0000139518.46032.e5.
- Susan L Hendrix 1, Amanda Clark, Ingrid Nygaard, Aaron Aragaki, Vanessa Barnabei, Anne Pelvic organ prolapse in the Women's Health Initiative: gravity and gravidityAm J Obstet Gynecol 2002 Jun;186(6):1160-6. doi: 10.1067/mob.2002.123819.
- J L Barnett 1, W L Hasler, M American Gastroenterological Association medical position statement on anorectal testing techniques. American Gastroenterological Association. Gastroenterology 1999 Mar;116(3):732-60. doi: 10.1016/s0016-5085(99)70194-0.
- Christopher Maher 1, Benjamin Feiner, Kaven Baessler, Corina Christmann-Schmid, Nir Haya, Jane Marjoribanks Transvaginal mesh or grafts compared with native tissue repair for vaginal prolapse Cochrane Database Syst Rev 2016 Feb 9;2(2):CD012079.
- Mickey Karram 1, Christopher Maher Surgery for posterior vaginal wall prolapse Int Urogynecol J 2013 Nov;24(11):1835-41. doi: 10.1007/s00192-013-2174-z.
- A C Richardson The rectovaginal septum revisited: its relationship to rectocele and its importance in rectocele repair Clin Obstet Gynecol 1993 Dec;36(4):976-83. doi: 1097/00003081-199312000-00022.
- Monique H Vaughan 1, Nazema Y Siddiqui, Laura K Newcomb, Alison C Weidner, Amie Kawasaki, Anthony G Visco, Megan S Bradley Surgical Alteration of Genital Hiatus Size and Anatomic Failure After Vaginal Vault Suspension Obstet Gynecol 2018 Jun;131(6):1137-1144. doi: 1097/AOG.0000000000002593.
- Megan S Bradley 1, Amy L Askew 2, Monique H Vaughan 3, Amie Kawasaki 3, Anthony G Visco 3 Robotic-assisted sacrocolpopexy: early postoperative outcomes after surgical reduction of enlarged genital hiatus Am J Obstet Gynecol 2018 May;218(5):514.e1-514.e8. doi: 1016/ j.ajog.2018.01.046. Epub 2018 Feb 6.
- John O.L. Delancey MD, William W. Hurd MD Size of the urogenital hiatus in the levator ani muscles in normal women and women with pelvic organ prolapse Obstetrics & Gynecology Volume 91, Issue 3, March 1998, Pages 364-368
- Christopher Maher Benjamin Feiner Kaven Baessler Corina Schmid Surgical management of pelvic organ prolapse in women Cochrane Database of Systematic Reviews
- Marie Fidela R. Paraiso MD, Matthew D. Barber MD, MHS, Tristi W. Muir MD, Mark D. Walters MD Rectocele repair: A randomized trial of three surgical techniques including graft augmentation American Journal of Obstetrics and Gynecology Volume 195, Issue 6, December 2006, Pages 1762-1771
Coordinadora:
Dra. Adelaida Garcia (Córdoba)
Mes Tocoginecologoga Encargada de Uroginecologia Hosp Rawson de Cordoba Miembro de la Comisión Directiva SOGC
Miembro de la Comisión directiva AUGA
Participantes:
Dr. Rene German Laurito (Rosario)
Tocoginecólogo.
Jefe de Sección Uroginecología Hospital Provincial del Centenario Rosario, Jefe de Departamento de Piso Pélvico Sanatorio de la Mujer Rosario.
Docente de Grado y Postgrado Universidad Nacional de Rosario. Prof. Adjunto de Ginecología UAI Rosario.
Miembro de CD Asoc. Uroginecológica Argentina (AUGA). Miembro CD Asoc. Obstetricia y Ginecología de Rosario (ASOGIR).
Dra. Lucila Pavan (Buenos Aires)
Médica ginecóloga especialista en Uroginecologia
Médica asociada del servicio de ginecología del Hospital Italiano de Buenos Aires
Dr. Gonzalo Martinez (Santiago del Estero)
Prof adjunto. Ginecologia Facultad ciencias médicas. UNSE
Médico de planta servicio ginecologia hospital independencia Sgo del Estero Médico de staff centro médico genesis
Miembro comision directiva de SACIG
Dr. Javier Vila (Neuquen)
Encargado de la sección de Uroginecologia del htal provincial Neuquén Profesor adjunto de la facultad de ciencias médicas universidad del comahue Miembro AUGA
SACIG
Dra. Marta Ledesma (Cordoba)
Especialista en Ginecología
Jefe Servicio Hospital Rawson Córdoba
Encargada de la Unidad piso pelviano, Centro Urologico Profesor Bengio Córdoba Docente Universidad Nacional Córdoba
Dra. Lorena Roca (San Juan)
Tocoginecóloga, con formación en uroginecología y rehabilitación Pelviperineal. Presidente de Asociación de ginecología y obstetricia de San Juan.
Jefe del sector de Uroginecologia y cirugía reconstructiva del Hospital Rawson San Juan
Dr. Mariano Rosini (Mar del Plata)
Encargado sección de Piso Pelvico de la Unidad Obstetrica y Ginecologica de Mar del Plata Miembro de AUGA
Dr. Santiago Orrico (Mendoza)
Jefe Unidad de Uroginecología Hospital Italiano. MENDOZA DOCENTE CÁTEDRA GINECOLOGÍA U. N. DE CUYO
Alcance del consenso: Médicos Toco ginecólogos Objetivos generales:
Desarrollar las patologías más prevalentes del piso de la pelvis
Establecer pautas de acción para el diagnóstico y propuesta terapéutica
Características generales del documento
El mismo se encuentra dividido en 5 ejes temáticos.
Avalado por la Asociación Uroginecologica Argentina (AUGA)